题目内容
目前市场上的手提应急灯,主要用的是“无液干粉”铅酸蓄电池,其原理是将强腐蚀性的浓硫酸灌注到硅胶中,使电解质溶液不易发生泄漏,大大改善了电池的性能.所用的原料仍然是Pb-PbO2-H2SO4,下列关于该铅酸蓄电池的说法正确的是( )
| A、充电时,电源的正极接蓄电池标“+”的一极,电池上标有“-”的一极发生氧化反应 |
| B、“无液干粉”铅酸蓄电池彻底改变了原来的铅酸蓄电池的原理 |
| C、放电时,在铅酸蓄电池的负极发生还原反应 |
| D、若用此铅酸蓄电池电解饱和NaCl溶液,标准状况下制备1.12LCl2,电池内至少消耗H2SO40.10 mol |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、充电过程是电解池,正极PbO2作阳极,负极铅作阴极;
B、“无液干粉”铅酸蓄电池和铅酸蓄电池的反应原理对比得出答案;
C、原电池的负极上发生失电子的氧化反应;
D、根据电解方程式结合电子守恒计算.
B、“无液干粉”铅酸蓄电池和铅酸蓄电池的反应原理对比得出答案;
C、原电池的负极上发生失电子的氧化反应;
D、根据电解方程式结合电子守恒计算.
解答:
解:A、充电时,电源的正极接蓄电池标“+”的一极,做电解池阳极,原电池中的负极铅连接标有“-”一极做电解池阴极,则电池上标有“-”的一极得电子发生还原反应,故A错误;
B、“无液干粉”铅酸蓄电池和原来的铅酸蓄电池的反应原理是一样的,故B错误;
C、放电时在铅酸蓄电池的负极发生氧化反应,故C错误;
D、标准状况下制备1.12LCl2,则氯气的物质的量为0.05mol,转移电子为0.1mol,铅酸蓄电池的反应为:PbO2+Pb+2H2SO4═2PbSO4+2H2O,所以转移电子为0.1mol,消耗硫酸0.1mol,故D正确.
故选:D.
B、“无液干粉”铅酸蓄电池和原来的铅酸蓄电池的反应原理是一样的,故B错误;
C、放电时在铅酸蓄电池的负极发生氧化反应,故C错误;
D、标准状况下制备1.12LCl2,则氯气的物质的量为0.05mol,转移电子为0.1mol,铅酸蓄电池的反应为:PbO2+Pb+2H2SO4═2PbSO4+2H2O,所以转移电子为0.1mol,消耗硫酸0.1mol,故D正确.
故选:D.
点评:本题考查学生二次电池铅蓄电池的工作原理知识,属于综合原电池和电解池工作原理知识的考查,侧重于基础知识的考查,题目难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
钢材可以用作桥梁的结构材料,是因为它( )
| A、有良好的导热性 |
| B、有一定的机械强度 |
| C、不易受空气和水的作用 |
| D、有良好的导电性 |
下列说法正确的是( )
| A、自发反应在任何条件下都能实现 |
| B、自发反应在恰当条件下才能实现 |
| C、凡是放热反应都是自发的,由于吸热反应都是非自发的 |
| D、自发反应一定是熵增大,非自发反应一定是熵减小或不变 |
根据下列三个反应方程式,判断下列关系正确的是( )
①I2+SO2+2H2O=H2SO4+2HI
②2FeCl3+2HI=2FeCl2+2HCl+I2
③2FeCl2+Cl2=2FeCl3.
①I2+SO2+2H2O=H2SO4+2HI
②2FeCl3+2HI=2FeCl2+2HCl+I2
③2FeCl2+Cl2=2FeCl3.
| A、氧化性:FeCl3>Cl2>H2SO4>I2 |
| B、还原性:SO2>HI>FeCl2>HCl |
| C、2Fe+3I2=2FeI3 |
| D、6FeI2+3Cl2=2FeCl3+4FeI3 |
从碘水中提取碘可供选择的试剂是( )
| A、苯、酒精 |
| B、汽油、酒精 |
| C、汽油、乙酸 |
| D、四氯化碳、苯 |
下列四个反应可用H++OH-=H2O表示的是( )
| A、氨水与盐酸反应 |
| B、向醋酸溶液中加入适量NaOH溶液 |
| C、稀硫酸与Ba(OH)2溶液反应 |
| D、NaOH溶液与稀硫酸反应 |
某兴趣小组以废弃的易拉罐、漂白粉、氢氧化钠等为原料制造了一种新型环保电池,并进行相关实验,如图所示.电池的总反应方程式为2Al+3ClO-+2OH-═3Cl-+2AlO2-+H2O.下列说法正确的是( )

| A、电池的负极反应式为:ClO-+H2O+2e-═Cl-+2OH- |
| B、当有0.1 mol Al完全溶解时,流经电解液的电子数为1.806×1023个 |
| C、往滤纸上滴加酚酞试液,b极附近颜色变红 |
| D、b极附近会生成蓝色固体 |
 一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,发生如下反应:CO (g) 十H2O (g)?CO2(g) 十 H2 (g);△H<0
一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,发生如下反应:CO (g) 十H2O (g)?CO2(g) 十 H2 (g);△H<0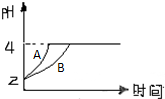 化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种,且均符合勒夏特列原理.
化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种,且均符合勒夏特列原理.