题目内容
一定条件下的密闭容器中有如下反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905.9kJ?mol-1,下列叙述正确的是( )
| A、4 mol NH3和5 mol O2反应,达到平衡时放出热量为905.9 kJ |
| B、平衡时v正(O2)=v逆(NO) |
| C、平衡后减小压强,混合气体平均摩尔质量增大 |
| D、平衡后升高温度,混合气体中NO含量降低 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A.减小压强,平衡向正反应方向移动;
B.达到平衡时,正逆反应速率相等;
C.反应为可逆反应,反应物不可能完全转化;
D.升高温度,平衡向逆反应方向移动.
B.达到平衡时,正逆反应速率相等;
C.反应为可逆反应,反应物不可能完全转化;
D.升高温度,平衡向逆反应方向移动.
解答:
解:A.反应为可逆反应,反应物不可能完全转化,则4mol NH3和5mol O2反应,达到平衡时放出热量小于905.9kJ,故A错误;
B.达到平衡时,正逆反应速率相等,应为v正(O2)=
v逆(NO),故B错误;
C.减小压强,平衡向正反应方向移动,混合气体平均摩尔质量减小,故C错误;
D.升高温度,平衡向逆反应方向移动,混合气体中NO含量降低,故D正确.
故选:D.
B.达到平衡时,正逆反应速率相等,应为v正(O2)=
| 5 |
| 4 |
C.减小压强,平衡向正反应方向移动,混合气体平均摩尔质量减小,故C错误;
D.升高温度,平衡向逆反应方向移动,混合气体中NO含量降低,故D正确.
故选:D.
点评:本题考查化学平衡的影响,题目难度中等,本题注意把握可逆反应的特点,注意外界条件对化学平衡的影响.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-=Mn2++Cl2↑+2H2O |
| B、硫酸溶液与氢氧化钡溶液混合:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| C、Cu溶于足量浓硝酸:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O |
| D、FeCl3溶液与Cu反应:Fe3++Cu=Fe2++Cu2+ |
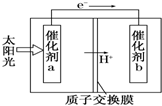 人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )| A、催化剂b表面的反应是CO2+2H++2e-═HCOOH |
| B、催化剂a表面发生氧化反应,有O2产生 |
| C、催化剂a附近酸性减弱,催化剂b附近酸性增强 |
| D、该过程是将太阳能转化为化学能的过程 |
化学与人类生活、社会可持续发展密切相关.下列说法不正确的是( )
| A、合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺的状况 |
| B、大量使用化肥和农药,以提高农作物产量 |
| C、含磷化合物的排放是“水华”和“赤潮”产生的原因 |
| D、安装煤炭“固硫”装置,降低酸雨发生率 |
有a L乙烯和乙炔的混合气体,与氢气发生加成反应时消耗氢气1.25a L,则混合气体中乙烯和乙炔的体积比是( )
| A、3:1 | B、4:1 |
| C、2:1 | D、1:1 |
 常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(气体体积已换算成标准状况下的体积),根据图中信息回答下列问题.
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(气体体积已换算成标准状况下的体积),根据图中信息回答下列问题.