题目内容
2.已知:Zn+CuSO4═ZnSO4+Cu将1.30克锌加入到足量的500mL0.10mol•L-1的CuSO4溶液中,当Zn完全反应后,计算反应后CuSO4溶液的物质的浓度(假设加入1.30锌后溶液的体积不变,请写出计算过程).
分析 n(Zn)=$\frac{1.30g}{65g/mol}$=0.02mol,n(CuSO4)=0.10mol/L×0.5L=0.05mol,根据方程式知,如果Zn完全反应需要硫酸铜0.02mol<0.05mol,所以硫酸铜有剩余,先根据Zn计算参加反应的硫酸铜的物质的量,再利用c=$\frac{n}{V}$计算反应后硫酸铜溶液物质的量浓度.
解答 解:n(Zn)=$\frac{1.30g}{65g/mol}$=0.02mol,n(CuSO4)=0.10mol/L×0.5L=0.05mol,根据方程式知,如果Zn完全反应需要硫酸铜0.02mol<0.05mol,所以硫酸铜有剩余,剩余硫酸铜的物质的量=(0.05-0.02)mol=0.03mol,则剩余溶液中硫酸铜物质的量浓度=$\frac{0.03mol}{0.5L}$=0.6mol/L,
答:反应后硫酸铜溶液的物质的量浓度是0.6mol/L.
点评 本题考查化学方程式的有关计算,为高频考点,正确判断哪种物质过量是解本题关键,注意:如果反应物都已知时一定要先进行过量计算,为易错点.

练习册系列答案
相关题目
12.在某容积一定的密闭容器中,可逆反应A(g)+B(g)?C(g)△H<0,符合图中(Ⅰ)所示关系,由此推断对图中(Ⅱ)的正确说法是( )


| A. | P3>P4,y轴表示A的转化率 | |
| B. | P3>P4,y轴表示B的质量分数 | |
| C. | P3>P4,y轴表示混合气体密度 | |
| D. | P3<P4,y轴表示混合气体的平均相对分子质量 |
13.矿石中金的含量很低,金的性质又相当稳定,只能用湿法冶金-氰化法提炼,及采用稀的NaCN溶液处理已粉碎的矿石,把少量的金浸取如溶液中,然后用金属锌作还原剂将金从溶液中置换析出,其反应原理为:
①4Au+8NaCN+O2+2H2O═4Na[Au(CN)2]+4NaOH
②2Na[Au(CN)2]+Zn═2Au+Na2[An(CN)4]
以下有关氰化法提炼金的说法中正确的是( )
①4Au+8NaCN+O2+2H2O═4Na[Au(CN)2]+4NaOH
②2Na[Au(CN)2]+Zn═2Au+Na2[An(CN)4]
以下有关氰化法提炼金的说法中正确的是( )
| A. | Na[Au(CN)2]可溶于水 | |
| B. | 化合物Na[Au(CN)2]中金元素的化合价为+2 | |
| C. | 金化学性质稳定,不与任何物质反应 | |
| D. | 在提炼过程中含金元素的物质始终作氧化剂 |
17.一定温度下,可逆反应3X(g)+Y(g)?2Z(g)达到平衡的标志是( )
| A. | 单位时间内生成n mol X,同时消耗3n molY | |
| B. | X的生成速率与Z的生成速率相等 | |
| C. | X、Y、Z的物质的量分数均保持不变 | |
| D. | X、Y、Z的分子个数比为3:1:2 |
14.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 80g CuO和Cu2S的混合物含有铜原子数一定为NA | |
| B. | 电解精炼铜时,当电路中转移NA个电子,阳极溶解32g铜 | |
| C. | 1mol铁与1molCl2充分反应,转移电子数为3NA | |
| D. | 向含有FeI2的溶液中通入适量氯气,当有1mol Fe2+被氧化时该反应转移电子的数目至少为NA |
11.下表为元素周期表短周期的一部分,下列有关X、Y、Z、W四种元素的叙述正确的是( )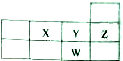

| A. | 原子半径大小:W>Y>X | B. | 核电荷数:W>Z>Y>X | ||
| C. | W的氧化物对应的水化物为强酸 | D. | X是ⅥA族元素,其最高化合价为+6价 |
12.下列离子在溶液中可以大量共存的一组是( )
| A. | Na+ NO3- SO42- | B. | Ag+ NO3- Cl- | ||
| C. | K+ H+ HCO3- | D. | NH4+ Na+ OH- |
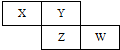 X、Y、Z、W四种短周期元素在周期表中的位置关系如图
X、Y、Z、W四种短周期元素在周期表中的位置关系如图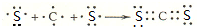 .
.
