题目内容
5.下列物质:①Na ②Cl2③Na2O2④NO2分别与水反应,氧化剂与还原剂的物质的量之比为1:1的是( )| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①②③④ |
分析 先根据元素化合价变化来确定氧化剂、还原剂,再根据方程式中氧化剂和还原剂的计量数之比判断即可.
解答 解:①2Na+2H2O=2NaOH+H2↑,该反应中钠是还原剂,水是氧化剂,氧化剂和还原剂的物质的量之比为1:1,故正确;
②Cl2+H2O=HCl+HClO中,氯元素的化合价由0价变为-1价和+1价,所以氧化剂和还原剂都是氯气,每个氯原子得电子或失电子个数相等,所以氧化剂和还原剂的物质的量之比为1:1,故正确;
③2Na2O2+2H2O=4NaOH+O2↑,该反应中氧元素的化合价由-1价变为0价和-2价,所以过氧化钠既是氧化剂又是还原剂,每个过氧化钠化学式中氧原子得失数相等,所以氧化剂和还原剂的物质的量之比为1:1,故正确;
④反应3NO2+H2O═2HNO3+NO,NO2为既是氧化剂,又是还原剂,参加反应的氧化剂与还原剂物质的量之比为1:2,故错误;
故选A.
点评 本题考查了氧化还原反应的有关计算,正确书写方程式是解本题关键,再根据方程式中各物理量的关系来分析解答,难度不大.

练习册系列答案
相关题目
15.下列说法正确的是( )
| A. | 因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 | |||||||||
| B. | 25℃、101kPa时,1mol S和2mol S的燃烧热不相等 | |||||||||
| C. | 通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能,例如:
| |||||||||
| D. | 任何化学反应都伴随着能量的变化 |
16.下列叙述正确的是( )
| A. | 用湿润的pH试纸测溶液的pH一定会有误差 | |
| B. | 用标准盐酸溶液滴定未知浓度的NaOH溶液时,用待测溶液润洗锥形瓶 | |
| C. | 用酸式滴定管量取酸性高锰酸钾溶液5.10mL | |
| D. | 用标准盐酸溶液滴定未知浓度NaOH溶液的过程中不慎将锥形瓶中的溶液溅出,会使测得的NaOH溶液的浓度偏大 |
13.下列说法或表示法错误的是( )
| A. | 吸热反应是由于反应物的总能量比生成物的总能量低 | |
| B. | 放热反应的△H>0 | |
| C. | 需要加热才能发生反应不一定是吸热反应 | |
| D. | 酸碱中和反应都是放热反应 |
20.830K时,在恒容密闭容器中进行的可逆反应:C(s)+H2O(g)?H2(g)+CO(g),下列哪种情况下,可说明该反应已经达到化学平衡状态( )
| A. | v正(C):v逆(H2)=1:1的状态 | |
| B. | 用H2O、CO、H2的物质的量浓度变化表示的反应速率的比为1:1:1的状态 | |
| C. | 混合气体的密度不再改变的状态 | |
| D. | 当平衡常数K不发生改变的时候 |
10.只含SiO2杂质的CaCO3样品,在高温煅烧后,残余物为一纯净物,则原样品中SiO2的质量分数是( )
| A. | 40% | B. | 28.6% | C. | 37.5% | D. | 62.5% |
17.下列各组物质中,仅用水及物质问互相反应就能区别的一组是( )
| A. | Na2O2 Al2(SO4)3 MgCl2 K2CO3 | B. | BaCl2 Na2SO4 CaCO3 KOH | ||
| C. | AgNO3 NaCl KCl CuCl2 | D. | Fe2(SO4)3 K2CO3 KHSO4 BaCl2 |
14.关于SO2的说法有:
①SO2是一种大气污染物;
②SO2和Cl2都有漂白作用,且这两种物质的漂白原理相同;
③工业上可用潮湿的石灰石粉末吸收SO2;
④SO2溶于水得硫酸,SO2是一种酸性氧化物;
⑤SO2是硫及某些含硫化合物在空气中燃烧的产物;
⑥SO2可以使酸性高锰酸钾溶液褪色,因为SO2具有漂白作用.
其中正确的是( )
①SO2是一种大气污染物;
②SO2和Cl2都有漂白作用,且这两种物质的漂白原理相同;
③工业上可用潮湿的石灰石粉末吸收SO2;
④SO2溶于水得硫酸,SO2是一种酸性氧化物;
⑤SO2是硫及某些含硫化合物在空气中燃烧的产物;
⑥SO2可以使酸性高锰酸钾溶液褪色,因为SO2具有漂白作用.
其中正确的是( )
| A. | ①②⑤ | B. | ①③④⑤ | C. | ①③⑤ | D. | ①③⑤⑥ |
15.某种硬铝合金是由 Al、Cu、Mg三种金属组成,主要应用于耐热可焊的结构件及锻件.某研究小组欲探究该合金的性质并测定合金中铝的质量分数:
(1)甲同学预测:该合金与10mol/L硝酸反应时有NO2气体生成,可能还有NO生成.
查阅资料:常温下,NO2与N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在.设计如下装置进行实验.按图连接装置并检验气密性后,称取5g 合金放于圆底烧瓶中,并滴加10mol/L硝酸.
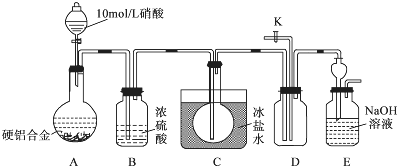
①合金中Cu与稀硝酸反应的离子方程式是3Cu+2NO3-+8H+=Cu2++2NO↑+4H2O.
②C装置的目的是将生成的NO2冷凝为N2O4,与NO分离,排除干扰.
③能证明有NO生成的实验操作与现象是打开活塞K,鼓入空气,若D中的气体由无色变为红棕色,证明有NO生成.
④实验进行至A中固体全部溶解后,未检验到有NO生成,甲同学认为硬铝合金与10mol/L硝酸反应时没有NO生成.乙同学认为不能确定是否生成了NO,需补充操作才能证明,该操作是在加入HNO3前,通入N2,除尽装置中的空气.
(2)为测定合金中铝的质量分数,丙同学查阅资料:
部分金属离子生成氢氧化物沉淀的pH
pH>7.8时,Al(OH)3开始溶解,pH>10.8时沉淀完全溶解.
设计如下方案并进行实验:

①调节pH时,应控制pH的范围是pH≥12.4.
②选用NaOH溶液调节pH,得到溶液B的离子方程式是Al3++4OH-=AlO2-+2H2O.
③Al(OH)3经过滤、洗涤、灼烧至恒重后称量,质量为8.5g,则该合金中铝的质量分数是90%.
(1)甲同学预测:该合金与10mol/L硝酸反应时有NO2气体生成,可能还有NO生成.
查阅资料:常温下,NO2与N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在.设计如下装置进行实验.按图连接装置并检验气密性后,称取5g 合金放于圆底烧瓶中,并滴加10mol/L硝酸.

①合金中Cu与稀硝酸反应的离子方程式是3Cu+2NO3-+8H+=Cu2++2NO↑+4H2O.
②C装置的目的是将生成的NO2冷凝为N2O4,与NO分离,排除干扰.
③能证明有NO生成的实验操作与现象是打开活塞K,鼓入空气,若D中的气体由无色变为红棕色,证明有NO生成.
④实验进行至A中固体全部溶解后,未检验到有NO生成,甲同学认为硬铝合金与10mol/L硝酸反应时没有NO生成.乙同学认为不能确定是否生成了NO,需补充操作才能证明,该操作是在加入HNO3前,通入N2,除尽装置中的空气.
(2)为测定合金中铝的质量分数,丙同学查阅资料:
部分金属离子生成氢氧化物沉淀的pH
| 金属离子 | 开始沉淀时的pH | 沉淀完全的pH |
| Al3+ | 3.4 | 4.7 |
| Cu2+ | 4.1 | 6.9 |
| Mg2+ | 9.4 | 12.4 |
设计如下方案并进行实验:

①调节pH时,应控制pH的范围是pH≥12.4.
②选用NaOH溶液调节pH,得到溶液B的离子方程式是Al3++4OH-=AlO2-+2H2O.
③Al(OH)3经过滤、洗涤、灼烧至恒重后称量,质量为8.5g,则该合金中铝的质量分数是90%.