题目内容
10.只含SiO2杂质的CaCO3样品,在高温煅烧后,残余物为一纯净物,则原样品中SiO2的质量分数是( )| A. | 40% | B. | 28.6% | C. | 37.5% | D. | 62.5% |
分析 只含SiO2杂质的CaCO3样品,在高温煅烧后,残余物为一纯净物,说明SiO2和CaCO3样品恰好完全反应生成CaSiO3,根据化学方程式:SiO2+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑可求.
解答 解:只含SiO2杂质的CaCO3样品,在高温煅烧后,残余物为一纯净物,说明SiO2和CaCO3样品恰好完全反应生成CaSiO3,SiO2+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑,则原样品中SiO2的质量分数为$\frac{60}{60+100}$×100%=37.5%,
故选C.
点评 本题考查了化学方程式的有关计算,难度不大,明确只含SiO2杂质的CaCO3样品,在高温煅烧后,残余物为一纯净物,说明SiO2和CaCO3样品恰好完全反应生成CaSiO3是关键.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
20.元素X的某价态离子Xn+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示.下列说法错误的是( )

| A. | 晶体中每个Xn+周围有2个等距离且最近的N3- | |
| B. | Xn+中n=l | |
| C. | 该晶体中阳离子与阴离子个数比为3:1 | |
| D. | X元素的原子序数是19 |
18.用酸性氢氧燃料电池为电源进行电解的实验装置示意图如图所示.下列说法中,正确的是( )
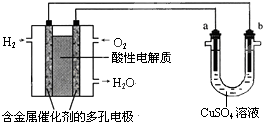

| A. | 燃料电池工作时,正极反应为:O2+4H+-4e-═2H2O | |
| B. | a极是粗铜,b极是纯铜,CuSO4溶液作电解质溶液时,CuSO4溶液浓度保持不变 | |
| C. | a、b两极均是石墨,CuSO4溶液作电解质溶液时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 | |
| D. | a极是铜,b极是铁,NaCl溶液作电解质溶液时铁受到保护,腐蚀速率减慢 |
5.下列物质:①Na ②Cl2③Na2O2④NO2分别与水反应,氧化剂与还原剂的物质的量之比为1:1的是( )
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①②③④ |
15.15g SiO2和足量的碳在高温下发生反应:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,下列叙述正确的是( )
| A. | 氧化剂和还原剂的质量比1:2 | B. | SiO2是还原剂 | ||
| C. | 反应中有6g碳被氧化 | D. | 反应中生成28gCO |
2.化学与生活密切相关,下列应用中利用了物质氧化性的是( )
| A. | 明矾净化水 | B. | 铁粉作食品袋内的脱氧剂 | ||
| C. | 食醋除水垢 | D. | 漂白粉漂白织物 |
19.下列离子或分子能够在指定的分散系中大量共存的是( )
| A. | 空气中:SO2、NO、N2、NH3 | |
| B. | 0.1mol/L的NaNO3溶液中:K+、I-、Cl-、SO42- | |
| C. | 铁与稀硫酸反应后的溶液中:[Fe(CN)6]3-、NH4+、Cl-、NO3- | |
| D. | 与铝反应生成大量氢气的溶液中:Mg2+、K+、HCO3-、NO3- |
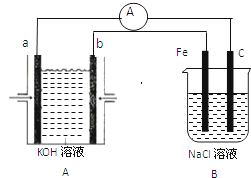 有图所示装置,装置A是氢氧燃料电池,已知该装置工作时电子从b极流向Fe电极.
有图所示装置,装置A是氢氧燃料电池,已知该装置工作时电子从b极流向Fe电极.