题目内容
15. 某实验小组对一含有Al3+的未知溶液进行了如下分析:
某实验小组对一含有Al3+的未知溶液进行了如下分析:(1)滴入少量氢氧化钠,无明显变化;
(2)继续滴加NaOH溶液,有沉淀生成;
(3)滴入过量的氢氧化钠,白色沉淀明显减少.实验小组经定量分析,得出如图所示沉淀与滴入氢氧化钠体积的关系.下列说法错误的是( )
| A. | 该未知溶液中一定含有Al3+ Mg2+ H+三种阳离子 | |
| B. | 滴加的NaOH溶液的物质的量浓度为5 mol•L-1 | |
| C. | 若将最终沉淀过滤、洗涤、灼烧,其质量可能为6 g | |
| D. | 若另一种离子为二价阳离子,则a=10 |
分析 A、依据实验过程分析滴入氢氧化钠无沉淀,说明含有H+,继续滴入氢氧化钠溶液生成白色沉淀说明一定生成氢氧化铝沉淀,说明溶液中含有Al3+,加入过量的氢氧化钠溶液沉淀减少,图象分析说明溶液中除了铝离子,应还有另一种金属阳离子;
B、依据图象分析溶解的氢氧化铝物质的量为0.20mol-0.15mol=0.05mol,消耗氢氧化钠溶液体积=110ml-100ml=10ml,氢氧化钠的浓度=$\frac{0.05mol}{0.01L}$=5mol/L;
C、最后得到的沉淀不能确定其成分,所以不能计算灼烧后得到的氧化物的质量,若果为氧化镁,按照方程式计算;
D、若另一种阳离子为二价金属阳离子,依据离子反应过程金属分析判断,氢氧化铝形成最大沉淀量0.05mol,二价金属物质的量为0.15mol,消耗氢氧化钠物质的量为0.05mol×3+0.15mol×2+a×10-3L×5mol/L=0.1L×5mol/L,a=10ml.
解答 解:A、实验过程分析滴入氢氧化钠无沉淀,说明含有H+,继续滴入氢氧化钠溶液生成白色沉淀说明一定生成氢氧化铝沉淀,说明溶液中含有Al3+,加入过量的氢氧化钠溶液沉淀减少,图象分析说明溶液中除了铝离子,应还有另一种金属阳离子,该未知溶液中至少含有3种阳离子,但不一定是镁离子,故A产错误;
B、依据图象分析溶解的氢氧化铝物质的量为0.20mol-0.15mol=0.05mol,消耗氢氧化钠溶液体积=110ml-100ml=10ml,氢氧化钠的浓度=$\frac{0.05mol}{0.01L}$=5mol/L,故B正确;
C、最后得到的沉淀不能确定其成分,若沉淀为氢氧化铝和氢氧化镁,根据原子守恒,则氧化铝为0.025mol,氧化镁为0.15mol,固体质量为0.025×102+0.15×40=6g,故C正确;
D、若另一种阳离子为二价金属阳离子,生成氢氧化铝最大沉淀量0.05mol,二价金属物质的量为0.15mol,开始消耗氢氧化钠体积为aml,消耗氢氧化钠物质的量为0.05mol×3+0.15mol×2+a×10-3L×5mol/L=0.1L×5mol/L,a=10,故D正确;
故选A.
点评 本题考查了图象分析的方法掌握,物质性质的分析应用,定量计算和图象中的定量分析是解题关键,题目难度较大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 某吸热反应能自发进行,因此该反应是熵增反应 | |
| B. | 已知NH4F水溶液中含有HF分子,因此NH4F溶液不能存放于玻璃试剂瓶中 | |
| C. | 可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 | |
| D. | 两种醋酸溶液的物质的量浓度分别c1和c2,pH分别为a和a+1,则c1=10c2 |
| A. | 中和反应是吸热反应 | |
| B. | 需要加热的反应都是吸热反应 | |
| C. | 断裂化学键要吸收能量 | |
| D. | 反应物总能量一定等于生成物总能量 |
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
| A. | 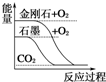 石墨转变成金刚石是吸热反应 | |
| B. | 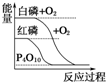 白磷比红磷稳定 | |
| C. | 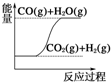 CO(g)+H2O(g)═CO2(g)+H2(g)△H>0 | |
| D. | 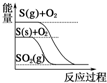 S(g)+O2(g)═SO 2(g)△H1 S(g)+O2((g)═SO2((g)△H2,则△H1>△H2 |
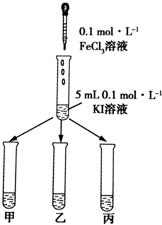 某学习小组通过下面的实验一和实验二,探究某些化学理论.
某学习小组通过下面的实验一和实验二,探究某些化学理论.实验一:以反应2Fe3++2I-=2Fe2++I2为例,
探究该反应是否为可逆反应.
实验方法:在KI溶液中滴加3mlFeCl3溶液,将混合液均
匀分到甲、乙、丙三支试管中;往试管甲中滴加淀粉
溶液,往试管乙中滴加KSCN溶液.如图所示:
(1)若试管甲中出现变蓝现象;
乙试管中出现血红色现象,
则说明该反应为可逆反应.
实验二:实验室制备CO2的反应.实验过程中的数据及相关信息如下表:
| 序号 | 反应温度/℃ | C(HCl)/mol•L-1 | V(HCl)/ml | 10g碳酸钙的形状 | t/min |
| ① | 20 | 2 | 10 | 块状 | t 1 |
| ② | 20 | 4 | 10 | 块状 | t 2 |
| ③ | 20 | 2 | 10 | 粉末 | t 3 |
| ④ | 40 | 2 | 10 | 粉末 | t 4 |
| ⑤ | 40 | 4 | 10 | 粉末 | t5 |
(2)由表格中的信息可知实验二的目的是探究影响化学反应速率的因素
(3)实验①和实验②是探究浓度对该化学反应速率的影响,分析表格中的信息可知,对该化学反应速率的影响因素还有温度、接触面积
(4)收集a ml CO2所需的时间最少的实验是⑤(填实验序号)
| A. | 热还原法 | B. | 电解法 | C. | 热分解法 | D. | 以上方法均不可 |
| A. | CH4 (g)+2O2(g)═CO2 (g)+2H2O(l)△H=a kJ•mol-1 CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=b kJ•mol-1 | |
| B. | 2H2(g)+O2(g)═2H2O(l)△H=a kJ•mol-1 H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=b kJ•mol-1 | |
| C. | C(s)+$\frac{1}{2}$O2 (g)═CO(g)△H=a kJ•mol-1 C(s)+O2(g)═CO2(g)△H=b kJ•mol-1 | |
| D. | S(g)+O2(g)═SO2 (g)△H=a kJ•mol-1 S(s)+O2(g)═SO2(g)△H=b kJ•mol-1 |
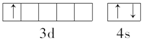 ,该元素基态原子结构示意图
,该元素基态原子结构示意图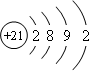 .该元素的名称为钪,形成的单质为金属晶体.
.该元素的名称为钪,形成的单质为金属晶体. 中心原子的杂化方式为
中心原子的杂化方式为