题目内容
11.对-甲基苯甲酸乙酯(F)是有机化工原料,用于合成药物的中间体,某兴趣小组利用中学的简单有机物进行合成,其方案如图: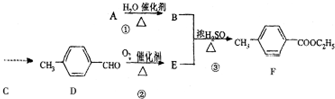
(1)A的结构简式是CH2=CH2,E中含有的官能团名称是羧基.
(2)指出化学反应类型:①加成反应;②氧化反应.
(3)丁子香酚(
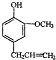 )是一种重要的调味剂,它与F的关系是b.
)是一种重要的调味剂,它与F的关系是b.a.同系物 b.同分异构体c.同种物质
(4)下列物质不能与丁子香酚发生反应的是bd.
a.NaOH溶液b.NaHCO3溶液c.Br2的四氯化碳溶液d.乙醇
(5)写出反应③的化学方程式:
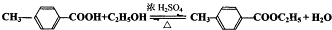 .
.
分析 (1)由F的结构可知,乙醇与 发生酯化反应生成F,由D的结构可知,E为
发生酯化反应生成F,由D的结构可知,E为 ,则B为CH3CH2OH,A与水发生加成反应生成B,则A为CH2=CH2;
,则B为CH3CH2OH,A与水发生加成反应生成B,则A为CH2=CH2;
(2)A的产量标志着一个国家石油化工发展水平,判断为乙烯,反应①是乙烯的水化加成反应生成乙醇,BE反应发生的酯化反应,判断反应②是催化氧化;
(3)结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物.互为同系物物质具有以下特点:结构相似、化学性质相似、分子式通式相同;分子式不同、物理性质不同;研究对象是有机物;具有相同分子式而结构不同的化合物互为同分异构体;组成和结构都相同的物质为同一物质,同一物质组成、结构、性质都相同,结构式的书写形式及物质的聚集状态可能不同;
(4)由丁子香酚的结构可知,分子中含有酚羟基,具有酚的性质,含有C=C双键,具有烯的性质等,据此解答;
(5)由(2)中分析可知,反应③是 与乙醇发生酯化反应生成
与乙醇发生酯化反应生成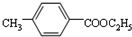 .
.
解答 解:由F的结构可知,乙醇与 发生酯化反应生成F,由D的结构可知,E为
发生酯化反应生成F,由D的结构可知,E为 ,则B为CH3CH2OH,A与水发生加成反应生成B,则A为CH2=CH2,
,则B为CH3CH2OH,A与水发生加成反应生成B,则A为CH2=CH2,
(1)由上述分析可知,A为CH2=CH2,E为 ,含有羧基,故答案为:CH2=CH2;羧基;
,含有羧基,故答案为:CH2=CH2;羧基;
(2)A的产量标志着一个国家石油化工发展水平,判断为乙烯,反应①是乙烯的水化加成反应生成乙醇,依据转化关系判断,B、E反应发生的是酯化反应,E中含有羧基,判断反应②是催化氧化;醛基被氧化为羧基;所以反应类型为:①加成反应; ②氧化反应;
故答案为:加成反应;氧化反应;
(3)丁子香酚(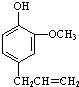 )含有酚羟基、醚键、碳碳双键,与F
)含有酚羟基、醚键、碳碳双键,与F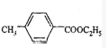 含有酯基,两者含有的官能团不同,结构不同、分子式相同,互为同分异构体,
含有酯基,两者含有的官能团不同,结构不同、分子式相同,互为同分异构体,
故答案为:b;
(4)由丁子香酚的结构可知,分子中含有酚羟基,能与NaOH反应,酸性比碳酸弱,不能与NaHCO3溶液反应,含有C=C双键,能与溴发生加成反应,不能与乙醇反应,
故答案为:bd;
(5)反应③是 与乙醇发生酯化反应生成
与乙醇发生酯化反应生成 ,反应方程式为
,反应方程式为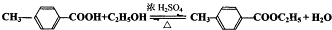 ,
,
故答案为: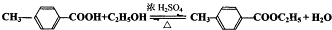 .
.
点评 本题考查了有机物的合成流程分析,物质官能团的判断和性质应用,同分异构体的书写方法,物质性质的熟练掌握是解题关键,官能团是解题的依据,题目难度中等.

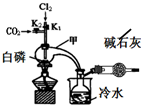 三氯化磷(PCl3)是合成药物的重要化工原料,可通过白磷和氯气化合得到.
三氯化磷(PCl3)是合成药物的重要化工原料,可通过白磷和氯气化合得到.已知:白磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;PCl3遇O2会生成POCl3(三氯氧磷);POCl3能溶于PCl3;POCl3和PCl3遇水会强烈水解.
实验室制取PCl3的装置示意图和有关数据如下:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 |
| 白磷 | 44.1 | 280.5 | 1.82 |
| PCl3 | -112 | 75.5 | 1.574 |
| POCl3 | 2 | 105.3 | 1.675 |
(1)实验所需氯气可用MnO2和浓HCl反应制取,实验过程中所用的玻璃仪器除酒精灯和玻璃导气管外,还需要的玻璃仪器有圆底烧瓶和分液漏斗.制取的氯气需要进行干燥,请设计实验证明通入的氯气是干燥的将氯气通入装有干燥的有色布条的集气瓶,布条不褪色,说明氯气是干燥的(写出操作、现象、结论).
(2)实验过程中要加入白磷、通入CO2、通入Cl2、加热,实验时具体的操作方法和顺序是先打开K2,等反应体系中充满CO2后,加入白磷,然后再打开K1,通入氯气,加热.
(3)E烧杯中加入冷水的目的是冷却收集PCl3,干燥管中碱石灰的作用是吸收多余的氯气和空气中的水蒸气.
(4)实验制得的粗产品中常含有POCl3、PCl5等,先加入过量白磷加热,除去PCl5和过量白磷后,再除去PCl3中的POCl3制备纯净的PCl3可选用的方法有C(填字母序号).
A.萃取 B.过滤 C.蒸馏 D.蒸发结晶
(5)①PCl3遇水会强烈水解生成H3PO3和HCl,则PCl3和水反应后所得溶液中除OH-之外其它离子的浓度由大到小的顺序是c(H+)>c(Cl-)>c(H2PO3-)>c(HPO32-)(已知亚磷酸(H3PO3)是二元弱酸).
②若将0.01mol POCl3投入热水配成1L的溶液,再逐滴加入AgNO3溶液,则先产生的沉淀是AgCl[已知Ksp(Ag3PO4)=1.4×10-16,Ksp(AgCl)=1.8×10-10].
| A. | 福尔马林(蚁酸):加入足量饱和碳酸钠溶液充分振荡,蒸馏,收集馏出物 | |
| B. | 乙醇(乙醛):加新制Cu(OH)2溶液,加热至沸腾,过滤取溶液 | |
| C. | 乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液,弃水层 | |
| D. | 苯(苯酚):加氢氧化钠溶液,充分振荡,分液,弃去下层液体 |
| A. | 该反应属于置换反应 | B. | 该反应的还原剂是NH3 | ||
| C. | Cl2的氧化性小于N2 | D. | 被氧化的NH3占参加反应NH3的1/4 |
| 化学键 | Si-Cl | H-H | H-Cl | Si-Si |
| 键能/KJ.mol | 360 | 436 | 431 | 176 |
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
(1)写出下列元素的名称:C钠,E氯
(2)B、C、D的简单离子半径由大到小的顺序是(用化学式表示)O2->Mg2+>Al3+
(3)①写出E单质与A、B、C形成的化合物反应的化学方程式Cl2+2OH-=Cl-+ClO-+H2O
②D单质与A、B、C形成的化合物的水溶液反应的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑
(4)用电子式表示C2B的形成过程
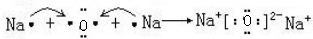 .
. | 元素 | W | Q | M | R | X | Y |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.112 | 0.102 | 0.066 |
| 主要化合价 | +1 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 原子半径:Y<M<Q,所以原子序数:Y>M>Q | |
| B. | M、Q、W都是金属,且其单质与盐酸反应的速率:M>Q>W | |
| C. | Q2+与X2-的电子层结构相同,且X2-离子半径大于Q2+ | |
| D. | M的氧化物能与W的最高价氧化物的水化物反应 |
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
 某同学通过如下实验,探究化学反应中的能量变化.
某同学通过如下实验,探究化学反应中的能量变化. ,用湿润的红色石蕊试纸检验该气体.
,用湿润的红色石蕊试纸检验该气体.