题目内容
16.已知键能数据:| 化学键 | Si-Cl | H-H | H-Cl | Si-Si |
| 键能/KJ.mol | 360 | 436 | 431 | 176 |
分析 化学反应方程式中的反应热=反应物的键能之和-生成物的键能之和.在硅晶体中每个硅原子和其它4个硅原子形成4个共价键,所以每个硅原子含有2个共价键.
解答 解:反应热=反应物的键能之和-生成物的键能之和,即△H=360kJ/mol×4+436kJ/mol×2-176kJ/mol×2-431kJ/mol×4=+236 kJ/mol,故答案为:+236KJ/mol.
点评 本题考查反应热的计算,题目侧重于反应热的计算,题目难度不大,注意原子晶体中键能的计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.分子式为C4H8烯烃的同分异构体(包括顺反异构)有( )种.
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
7.某同学为了测定三聚氰胺的分子式和结构简式,设计了如下实验:
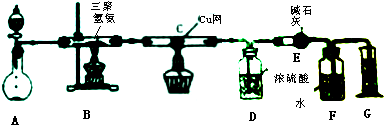
查阅资料,三聚氰胺的相对分子质量为126,三聚氰胺在常温下成晶体,在加热条件下能与氧气发生反应生成二氧化碳、氮气和水.取12.6g的三聚氰胺晶体如图装置进行实验(假设三聚氰胺完全反应转化产物).
(1)抑制A装置中固体为Na2O2,请写出其中发生反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑;
(2)D装置不能与E装置互换的理由是浓硫酸吸水,碱石灰吸收二氧化碳,若互换位置,则碱石灰会同时吸收水和二氧化碳,导致实验失败;
(3)当B装置中反应完全发生后,读取G中的体积的使用操作顺序为②③①(填序号).
①读数②冷却至室温③调平F、G装置中的液面
(4)测定数据如下:
经测定,F中收集的气体折合标准状况下的体积为6.72L.
①利用上述实验数据,计算三聚氰胺的量筒式为CN2H2;
②三聚氰胺的分子式为C3N6H6;
③若没有C装置中的铜网,对测定结果的影响是测定所得分子式的氮原子数偏大,而碳、氢原子数偏小.

查阅资料,三聚氰胺的相对分子质量为126,三聚氰胺在常温下成晶体,在加热条件下能与氧气发生反应生成二氧化碳、氮气和水.取12.6g的三聚氰胺晶体如图装置进行实验(假设三聚氰胺完全反应转化产物).
(1)抑制A装置中固体为Na2O2,请写出其中发生反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑;
(2)D装置不能与E装置互换的理由是浓硫酸吸水,碱石灰吸收二氧化碳,若互换位置,则碱石灰会同时吸收水和二氧化碳,导致实验失败;
(3)当B装置中反应完全发生后,读取G中的体积的使用操作顺序为②③①(填序号).
①读数②冷却至室温③调平F、G装置中的液面
(4)测定数据如下:
| 装置 | D | E |
| 实验前 | 101.0g | 56.0g |
| 实验后 | 106.4g | 69.2g |
①利用上述实验数据,计算三聚氰胺的量筒式为CN2H2;
②三聚氰胺的分子式为C3N6H6;
③若没有C装置中的铜网,对测定结果的影响是测定所得分子式的氮原子数偏大,而碳、氢原子数偏小.
4.下列表示正确的是( )
| A. | 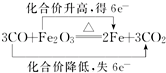 | B. |  | ||
| C. | 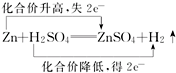 | D. | 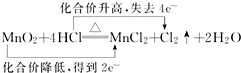 |
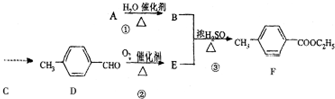
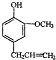 )是一种重要的调味剂,它与F的关系是b.
)是一种重要的调味剂,它与F的关系是b.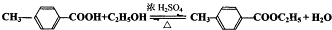 .
.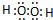 ,该分子含有极性键和非极性键(填“极性”、“非极性”)键
,该分子含有极性键和非极性键(填“极性”、“非极性”)键