题目内容
1.某元素质量数52,中子数28,其基态原子未成对电子数为( )| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
分析 质量数=质子数+中子数,质量数52,中子数28,则该元素原子的质子数为52-28=24,根据核外电子排布规律书写基态原子的电子排布式,据此判断.
解答 解:质量数52,中子数28,则该元素原子的质子数=质量数-中子数=52-28=24,
故该元素基态原子的电子排布式为:1s22s22p63s23p63d54s1,3d能级具有5个轨道,4个电子优先分别占据1个轨道,且自旋方法相同,故有6个成对电子,
故选D.
点评 本题考查核外电子排布规律等,题目难度不大,理解核外电子排布规律,掌握核外电子排布规律是解题的关键.

练习册系列答案
相关题目
12.下列化学反应中,光照对它几乎没有影响的是( )
| A. | 氯气与氢气的反应 | B. | 氯气与甲烷的反应 | ||
| C. | 次氯酸的分解反应 | D. | 甲烷的分解反应 |
9.下列化学反应中水作氧化剂的是( )
| A. | SO2+H2O | B. | Fe+H2O | C. | Cl2+H2O | D. | NO2+H2O |
6.环境污染已成为人类社会面临的重大威胁,下列各项中与环境污染无关的是( )
①温室效应;②赤潮;③酸雨;④光化学污染;⑤臭氧空洞;⑥工业含汞水排放;⑦潮汐现象; ⑧水华;⑨地方性甲状腺肿大.
①温室效应;②赤潮;③酸雨;④光化学污染;⑤臭氧空洞;⑥工业含汞水排放;⑦潮汐现象; ⑧水华;⑨地方性甲状腺肿大.
| A. | ⑥⑧ | B. | ④⑤ | C. | ①②③ | D. | ⑦⑨ |
10.下列分子式一定表示纯净物的是( )
| A. | C4H10 | B. | C3H8 | C. | C5H12 | D. | C3H7Cl |
11.已知25℃时:
①HF(aq)+OH-(aq)═F-(aq)+H2O(l)△H1=-67.7kJ•mol-1
②H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ•mol-1
③Ba2+(aq)+SO42-(aq)═BaSO4(s)△H3<0
下列说法正确的是( )
①HF(aq)+OH-(aq)═F-(aq)+H2O(l)△H1=-67.7kJ•mol-1
②H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ•mol-1
③Ba2+(aq)+SO42-(aq)═BaSO4(s)△H3<0
下列说法正确的是( )
| A. | HF的电离方程式及热效应:HF(aq)═H+(aq)+F-(aq)△H>0 | |
| B. | 在氢氧化钠溶液与盐酸的反应中,盐酸量一定,氢氧化钠溶液量越多,中和热越大 | |
| C. | △H2=-57.3 kJ•mol-1是强酸和强碱在稀溶液中反应生成可溶盐的中和热 | |
| D. | 稀硫酸与稀氢氧化钡溶液反应的热化学方程式为:H2SO4(aq)+Ba(OH)2(aq)═BaSO4(s)+2H2O(l)△H=-114.6 kJ•mol-1 |
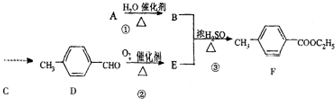
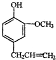 )是一种重要的调味剂,它与F的关系是b.
)是一种重要的调味剂,它与F的关系是b.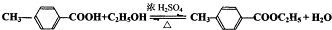 .
.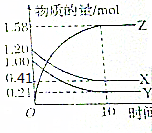 (1)在两个恒温、恒容的密闭容器中进行下列两个可逆反应:
(1)在两个恒温、恒容的密闭容器中进行下列两个可逆反应: