题目内容
化学式为C5H12O的醇的同分异构体有( )
| A、6种 | B、7种 | C、8种 | D、9种 |
考点:同分异构现象和同分异构体
专题:
分析:先书写戊基-C5H11异构体,戊基异构数目等于戊醇的异构体数目.
解答:
解:戊基-C5H11可能的结构有:-CH2CH2CH2CH2CH3、-CH(CH3)CH2CH2CH3、-CH(CH2CH3)2、-CHCH(CH3)CH2CH3、-C(CH3)2CH2CH3、-C(CH3)CH(CH3)2、-CH2CH2CH(CH3)2、-CH2C(CH3)3,则戊醇的可能结构有8种,故选C.
点评:本题注意考查有机物的推断、同分异构体的书写等,难度中等,注意确定的方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关实验仪器的使用及实验操作正确的是( )
| A、蒸发皿和烧杯均可用于加热 |
| B、为减少仪器使用而带来的误差,中和热测定实验中可用温度计兼做搅拌棒 |
| C、配置1L0.1mol?L-1NaCl溶液的实验中,用托盘天平称取5.85gNaCl |
| D、测定溶液中草酸含量时,用碱式滴定管盛装KMnO4标准液进行滴定操作 |
下列反应中不属于水解反应的是( )
| A、纤维素在稀硫酸作用下转化为葡萄糖 |
| B、葡萄糖在酒化酶作用下转化为乙醇和二氧化碳 |
| C、油脂在氢氧化钠溶液中加热发生皂化反应 |
| D、麦芽糖在一定条件下转化为葡萄糖 |
下列说法正确的是( )
| A、一定温度下,反应MgCl2(s)═Mg(s)+Cl2(g)的△H<0△S>0 |
| B、氨气分解反应 2NH3?N2+3H2 达到平衡后,升高温度平衡逆向移动 |
| C、铅蓄电池放电时的负极和充电时的阳极均发生还原反应 |
| D、对于反应2H2O2═2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 |
下列有关说法正确的是( )
| A、相同类型的离子晶体,晶格能越大,形成的晶体越稳定 |
| B、中心原子的杂化方式取决于其配位原子的数目 |
| C、用金属的电子气理论能合理的解释金属易腐蚀的原因 |
| D、H3O+、NH4Cl和[Ag(NH3)2]+中均存在配位键 |
形成原电池的条件一般有:①电解质溶液②两个电极③能自发地发生氧化还原反应④形成闭合回路
请根据上述条件判断下列装置中属于原电池的是( )
请根据上述条件判断下列装置中属于原电池的是( )
A、 NaCl溶液 |
B、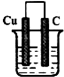 HCl溶液 |
C、 CuSO4溶液 |
D、 蔗糖溶液 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、标准状况下,2.24L苯中含C-H数目为0.6 NA |
| B、常温下,9.2gNO2和N2O4的混合气体中含有的氮原子数目为0.2NA |
| C、常温下,1.0LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
| D、在反应KClO3+6HCl═KCl+3Cl2↑+3H2O中,每生成3molCl2转移的电子数为6NA |



