题目内容
19.欲配制100mL 1.0mol•L-1Na2SO4溶液,正确的方法是( )①将14.2g Na2SO4溶于100mL水中
②将32.2gNa2SO4•10H2O溶于少量水 中,再用水稀释至100mL
③将20mL 5.0mol•L-1Na2SO4溶液用水稀释至100mL.
| A. | ①② | B. | ②③ | C. | ① | D. | ①②③ |
分析 欲配制100mL 1.0mol•L-1Na2SO4溶液,用固体配制时依据m=CV计算需要溶质的质量,加水稀释到100mL;
用浓溶液配制,依据溶液稀释规律:稀释前后溶质的物质的量不变计算需要浓溶液体积,然后加水稀释都100mL.
解答 解:①配制100mL 1.0mol•L-1Na2SO4溶液,需要溶质Na2SO4的质量为1.0mol/L×0.1L×142g/mol=14.2g,溶于100mL水中,则溶液体积大于100mL,溶液浓度小于1.0mol/L,故错误;
②配制100mL 1.0mol•L-1Na2SO4溶液,需要溶质Na2SO4的质量为1.0mol/L×0.1L×322g/mol=32.2g,溶于少量水中,再用水稀释至100mL,故正确;
②配制100mL 1.0mol•L-1Na2SO4溶液,设需要5.0mol•L-1Na2SO4体积为V,则依据稀释前后溶质的物质的量不变,设需要浓溶液体积为V,则100mL×1.0mol/L=5.0mol/L×V,解得V=20mL,稀释后溶液体积为100mL,故正确;
故选:B.
点评 本题考查配制一定物质的量浓度的溶液的配制,准确把握物质的量浓度含义是解题关键,注意分清溶液体积和溶剂体积,题难度不大.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
9.下列说法正确的是( )
| A. | 检验某酸性溶液中Cl-和SO42-,选用试剂及顺序是过量Ba(NO3)2溶液、AgNO3溶液 | |
| B. | 将足量CO2和SO2的混合气体分别通入BaCl2溶液、Ba(NO3)2溶液中,最终都无沉淀生成 | |
| C. | 将铁粉加入FeCl3、CuCl2混合溶液中,充分反应后剩余的固体中必有铁 | |
| D. | 用加热分解的方法可将NH4Cl固体和Ca(OH)2固体的混合物分离 |
7.对气体反应:mA+nB?eC,温度(T)、压强(P)、时间(t)与生成物的体积百分数C%的关系图,下列结论正确的是( )
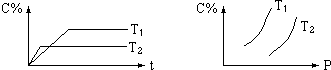
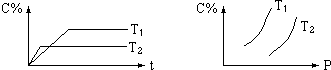
| A. | T1<T2 | B. | m+n<e | ||
| C. | 正反应是吸热反应 | D. | 逆反应是放热反应 |
14.有八种物质:①甲烷 ②苯 ③聚乙烯 ④聚异戊二烯 ⑤2-丁炔 ⑥环己烷 ⑦邻二甲苯⑧环己烯,既能使KMnO4酸性溶液褪色,又能与溴水反应使之褪色的是( )
| A. | ①④⑤⑧ | B. | ②④⑤⑦⑧ | C. | ④⑤⑧ | D. | ③④⑤⑦⑧ |
4.下列有关物质的性质或应用的说法正确的是( )
| A. | 在甲苯中加入少量酸性高锰酸钾溶液,振荡后褪色,正确的解释是由于侧链与苯环的相互影响,使侧链和苯环均易被氧化 | |
| B. | 等质量的乙烷、乙烯、乙炔在氧气中完全燃烧,乙烷消耗的氧气最多 | |
| C. | 间二溴苯仅有一种空间结构可证明苯分子中不存在单双键交替的结构 | |
| D. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
8.人体内葡萄糖的消耗可用下列热化学方程式表示:C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(l)△H=-2800kJ•mol-1;如果某人每天消耗12600kJ热量,则他每天至少要摄入葡萄糖的质量为( )
| A. | 4.5 g | B. | 810 g | C. | 1250 g | D. | 900 g |
9.下列各组离子,在溶液中可以大量共存的是( )
| A. | H+、SO42-、CO32-、K+ | B. | Fe3+、Na+、OH-、NO3- | ||
| C. | Mg2+、Al3+、Cl-、SO42- | D. | Na+、Cl-、OH-、NH4+ |