题目内容
7.对气体反应:mA+nB?eC,温度(T)、压强(P)、时间(t)与生成物的体积百分数C%的关系图,下列结论正确的是( )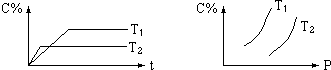
| A. | T1<T2 | B. | m+n<e | ||
| C. | 正反应是吸热反应 | D. | 逆反应是放热反应 |
分析 先拐先平数值大,T1<T2,升高温度平衡时C%减少,平衡逆向移动,说明逆反应是吸热反应,由右图可知,增大压强,平衡时C%增大,平衡是正向移动,则正反应方向为气体体积减小的方向.
解答 解:先拐先平数值大,T1<T2,升高温度平衡时C%减少,平衡逆向移动,说明逆反应是吸热反应,则正反应是放热反应;
由右图可知,增大压强,平衡时C%增大,平衡是正向移动,则正反应方向为气体体积减小的方向,因此m+n>e,
故选A.
点评 本题考查了化学平衡图象,难度中等,为高考高频考点,掌握外界条件对化学平衡的影响是解题关键.

练习册系列答案
相关题目
17.下列各组溶液,不用外加试剂,就能实现鉴别的是( )
①CuSO4 K2SO4 KNO3 KOH ②Na2CO3 BaCl2 HCl Na2SO4
③NH4NO3 Na2SO4 Ba(OH)2 AlCl3 ④NaAlO2 Na2SiO3 H2SO4 NaCl.
①CuSO4 K2SO4 KNO3 KOH ②Na2CO3 BaCl2 HCl Na2SO4
③NH4NO3 Na2SO4 Ba(OH)2 AlCl3 ④NaAlO2 Na2SiO3 H2SO4 NaCl.
| A. | ①③ | B. | ②④ | C. | ①③④ | D. | ②③④ |
18.将0.4molAgNO3,0.8mol Cu(NO3)2,0.8molKCl液1L用惰性电极电解一段时间后,在一个电极上析出0.3molCu,此时在另 一个电极上放出气体的体积(标准状况)约为( )
| A. | 5.6L | B. | 6.72L | C. | 2.8L | D. | 13.44L |
12.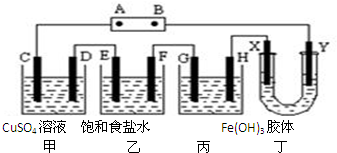 将下列装置如图连接,D、F、X、Y、E 都是铂电极,C是铁电极.甲,乙,丙三个装置中电解前后溶液的体积都是500mL.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.下列说法不正确的是( )
将下列装置如图连接,D、F、X、Y、E 都是铂电极,C是铁电极.甲,乙,丙三个装置中电解前后溶液的体积都是500mL.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.下列说法不正确的是( )
 将下列装置如图连接,D、F、X、Y、E 都是铂电极,C是铁电极.甲,乙,丙三个装置中电解前后溶液的体积都是500mL.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.下列说法不正确的是( )
将下列装置如图连接,D、F、X、Y、E 都是铂电极,C是铁电极.甲,乙,丙三个装置中电解前后溶液的体积都是500mL.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.下列说法不正确的是( )| A. | 电源B 极的名称是负极,丁中Y极附近颜色变深 | |
| B. | 乙装置中电解一段时间后,加入0.2mol盐酸则可以恢复原来的浓度 | |
| C. | 设甲池中溶液的体积在电解前后都是500ml,当乙池所产生气体的体积为4.48L(标准状况)时,甲池中所生成物质的物质的量浓度为0.2mol/L | |
| D. | 甲装置中电解反应的总化学方程式是:CuSO4+Fe$\frac{\underline{\;电解\;}}{\;}$Cu+FeSO4 |
19.欲配制100mL 1.0mol•L-1Na2SO4溶液,正确的方法是( )
①将14.2g Na2SO4溶于100mL水中
②将32.2gNa2SO4•10H2O溶于少量水 中,再用水稀释至100mL
③将20mL 5.0mol•L-1Na2SO4溶液用水稀释至100mL.
①将14.2g Na2SO4溶于100mL水中
②将32.2gNa2SO4•10H2O溶于少量水 中,再用水稀释至100mL
③将20mL 5.0mol•L-1Na2SO4溶液用水稀释至100mL.
| A. | ①② | B. | ②③ | C. | ① | D. | ①②③ |
16.现有氧化铝、石灰石、二氧化硅三种白色粉末,若用一种试剂将它们区别开来,此试剂是( )
| A. | 水 | B. | 盐酸 | C. | 氢氧化钠溶液 | D. | 硝酸银溶液 |