题目内容
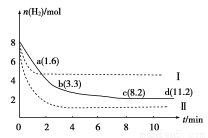
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是CO2(g)+3H2(g)? CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,某科学实验将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后数字表示对应的坐标):下列说法不正确的是
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,某科学实验将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后数字表示对应的坐标):下列说法不正确的是
A.该反应在低温条件下能自发进行
B.曲线Ⅰ改变的条件可能是升高温度
C.若实线对应条件下平衡常数为K,曲线Ⅰ对应条件下平衡常数为K1,曲线Ⅱ对应条件下平衡常数为K2,则K、K1和K2的大小关系是:K2 >K > K1
D.容器内气体平均摩尔质量不再改变说明该反应达到平衡状态
C
【解析】
试题分析:A、根据ΔG=ΔH-TΔS<0,反应自发进行判断,该反应的ΔS<0,ΔH<0,所以该反应低温时自发进行,正确;B、若升高温度,反应速率加快,到达平衡的时间缩短,平衡逆向移动,氢气的物质的量增加,正确;C、由图像可知,与实线相比,曲线I代表温度升高,曲线II平衡时氢气的物质的量减少,但达到平衡的时间缩短,所以曲线II表示的是增大压强,平衡正向移动,反应速率加快,而该反应是放热反应,温度高,平衡常数减小,温度不变,平衡常数不变,所以三者的关系是 K2 =K > K1,错误;D、该反应是气体的物质的量发生改变的可逆反应,气体的总质量不变,所以气体的平均摩尔质量在变化,达平衡时不再变化,正确,答案选C。
考点:考查对化学平衡图像的分析与判断,平衡常数的判断

无色溶液中含有:①Na+、②Ba2+、③C1—、④Br—、⑤SO32-、⑥SO42-、⑦Fe2+离子中的一种或几种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
步骤 | 操作 | 现象 |
① | 用pH试纸检验 | 溶液的pH大于7 |
② | 向溶液中滴加氯水,再加入CC14振荡,静置 | CC14层呈橙红色 |
③ | 取②的上层溶液,加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
④ | 将③过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
根据上述实验现象,判断以下结论中正确的是
A.肯定含有的离子是①④⑤ B.肯定没有的离子是②⑤⑦
C.可能含有的离子是①②⑥ D.不能确定的离子是①③⑥

