题目内容
氧化还原反应实际上包含氧化和还原两个过程。(1)向氯酸钠(NaClO3)的酸性水溶液中通入二氧化硫,该反应中氧化过程的反应式为:SO2+2H2O – 2e → SO42- + 4H+; (2)向亚氯酸钠(NaClO2)固体中通入用空气稀释的氯气,该反应中还原过程的反应式为:Cl2 + 2e → 2Cl-。在(1)和(2)反应中均会生成产物X,则X的化学式为
A.NaClO B.NaClO4 C.HClO D.ClO2
D
【解析】
试题分析:(1)中S元素的化合价升高,则Cl元素的化合价降低,反应后Cl元素的化合价小于+5价;(2)中还原过程的反应式为:Cl2+2e-→2Cl-,则亚氯酸钠(NaClO2)Cl元素的化合价升高,反应后Cl元素的化合价大于+3价,又在(1)和(2)反应中均会生成产物X,X中Cl元素的化合价在+3~+5价之间,只有ClO2符合,其Cl元素的化合价为+4价,故D项正确。
考点:本题考查氧化还原反应原理。

 阅读快车系列答案
阅读快车系列答案(18分)某校化学实验兴趣小组在“探究卤索单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入l~2滴溴水,振荡后溶液呈黄色。
提出问题 Fe3+、Br2谁的氧化性更强?
(1 )猜 想: ①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含 (填化学式,下同)所致。
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含 所致。
(2)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。
供选用的试剂:a.酚酞试液;b.CCl4;c.无水酒精;d.KSCN溶液。
请你在下表中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
| 选用试剂 | 实验现象 |
方案1 |
|
|
方案2 |
|
|
(3)结论:氧化性:Br2>Fe3+。故在足量的稀氯化亚铁溶液中,加入l~2滴溴水,溶液呈黄色所发生的离子反应方程式为 。
(4)实验后的思考
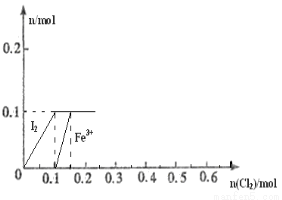
①根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是:
(填离子的化学式)。
②在100 mL FeBr2溶液中通入2.24 L Cl2(标准状况),溶液中有1/2的Br-被氧气成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为 。
 NaAlO2(aq)
NaAlO2(aq) Al(OH)3 ②S
Al(OH)3 ②S SO3
SO3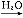 H2SO4
H2SO4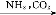 NaHCO3
NaHCO3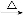 Na2CO3
Na2CO3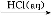 FeCl3(aq)
FeCl3(aq) Mg(OH)2
Mg(OH)2 MgO
MgO 、SO
、SO 、Na+,向其中加入Na2O2后,溶液中浓度基本保持不变的离子是
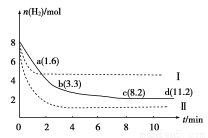
、Na+,向其中加入Na2O2后,溶液中浓度基本保持不变的离子是 CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,某科学实验将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后数字表示对应的坐标):下列说法不正确的是
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,某科学实验将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后数字表示对应的坐标):下列说法不正确的是