题目内容
下列实验的操作和所用的试剂都正确的是( )
| A、要鉴别己烯中是否混有少量甲苯,应先加足量溴水,然后再加入酸性高锰酸钾溶液 |
| B、配制浓硫酸和浓硝酸的混酸时,将浓硝酸沿壁缓缓倒入到浓硫酸中 |
| C、除去溴苯中少量的溴,可以加水后分液 |
| D、制硝基苯时,将盛有混合液的试管直接在酒精灯火焰上加热 |
考点:化学实验方案的评价,有机物的鉴别,溶液的配制,物质的分离、提纯和除杂
专题:实验评价题
分析:A.己烯、甲苯都可与酸性高锰酸钾发生氧化还原反应,为避免干扰,应先除去己烯;
B.加入酸液时,应避免酸液飞溅;
C.溴易溶于溴苯,应加入氢氧化钠溶液除杂;
D.制取硝基苯,应水浴加热.
B.加入酸液时,应避免酸液飞溅;
C.溴易溶于溴苯,应加入氢氧化钠溶液除杂;
D.制取硝基苯,应水浴加热.
解答:
解:A.应先加足量溴水,己烯与溴发生加成反应,然后再加入酸性高锰酸钾溶液,可检验甲苯,故A正确;
B.加入酸液时,应避免酸液飞溅,应将浓硫酸加入到浓硝酸中,故B错误;
C.溴易溶于溴苯,应加入氢氧化钠溶液除杂,故C错误;
D.制取硝基苯,加入温度为50~60℃,应水浴加热,故D错误.
故选A.
B.加入酸液时,应避免酸液飞溅,应将浓硫酸加入到浓硝酸中,故B错误;
C.溴易溶于溴苯,应加入氢氧化钠溶液除杂,故C错误;
D.制取硝基苯,加入温度为50~60℃,应水浴加热,故D错误.
故选A.
点评:本题考查较为综合,涉及物质的分离、提纯、检验和鉴别,为高频考点,侧重于学生的分析能力、实验能力的考查,注意把握物质的性质的异同,以及实验的严密性、可行性的评价,难度不大.

练习册系列答案
 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
下列变化中反应物作氧化剂的是( )
| A、MnO4→Mn2+ |
| B、HCl→Cl2 |
| C、Fe→Fe3+ |
| D、KClO3→O2 |
在50ml0.01mol/LH2SO4溶液加入50ml0.01mol/LNaOH溶液时,所得溶液呈( )
| A、无法判断 | B、碱性 |
| C、中性 | D、酸性 |
已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH值:
下列说法或表达正确的是( )
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
| A、2NaClO+CO2+H2O→Na2CO3+2HClO |
| B、HCN+Na2CO3→NaHCO3+NaCN |
| C、常温下电离常数:Ki2(H2CO3)>Ki(C6H5OH)>Ki(HCN) |
| D、结合质子能力的强弱顺序为:CO32-<HCO3-<CH3COO- |
pH=2的强酸溶液,加水稀释,若溶液体积扩大10倍,则C(H+)或C(OH-)的变化( )
| A、c(H+)和c(OH-)都减少 |
| B、c(H+)增大 |
| C、c(OH-)减小 |
| D、c(H+)减小 |
如图装置或操作能达到相应实验目的是( )
A、 制取少量氨气 |
B、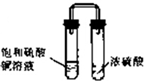 放置一段时间后,饱和硫酸铜溶液中出现蓝色晶体 |
C、 继续煮沸溶液至红褐色沉淀,停止加热,当光束通过体系时一定可产生丁达尔效应 |
D、 将海带灼烧成灰 |
a g Fe粉与一定量的硝酸在一定条件下充分反应,将生成的气体与标准状况下b L O2混合,恰好能被水完全吸收,则a和b的关系可能是( )
| A、b>0.3a |
| B、b<0.2a |
| C、0.2a≤b≤0.3a |
| D、无法确定 |
下列说法中不正确的是( )
| A、任何可燃性气体点燃前必须要验纯 |
| B、在实验室可通过品尝的方法来鉴别食盐与葡萄糖两种白色固体 |
| C、容量瓶、分液漏斗使用前需查漏 |
| D、氢氧化钠溶液沾到皮肤上后应立即用大量水冲洗 |