题目内容
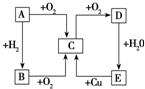 如图所示,A、B、C、D、E五种物质的相互转化关系
如图所示,A、B、C、D、E五种物质的相互转化关系请完成下列问题:
(1)若A通常状态下为固态单质,则分别为(写化学式):A
(2)若A通常状态下为气态单质,则分别为(写化学式):A
考点:无机物的推断
专题:
分析:(1)当A是固体单质时,A能与氧气、氢气反应,且B能发生连续氧化反应,则A为S,B为H2S,C为SO2,D为SO3,E为H2SO4;
(2)若A通常状态下为气体单质,根据转化关系知,C是NO,A和氧气反应生成NO,A是N2,氮气和氢气生成氨气,则B是NH3,D为NO2,二氧化氮和水反应生成硝酸和NO,E能和Cu反应生成NO,则E是HNO3,以此解答该题.
(2)若A通常状态下为气体单质,根据转化关系知,C是NO,A和氧气反应生成NO,A是N2,氮气和氢气生成氨气,则B是NH3,D为NO2,二氧化氮和水反应生成硝酸和NO,E能和Cu反应生成NO,则E是HNO3,以此解答该题.
解答:
解:(1)当A是固体单质时,A能与氧气、氢气反应,且B能发生连续氧化反应,则A为S,B为H2S,C为SO2,D为SO3,E为H2SO4,由E生成C反应的化学方程式是Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,
故答案为:S;H2S;SO3;Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
(2)若A通常状态下为气体单质,根据转化关系知,C是NO,A和氧气反应生成NO,A是N2,氮气和氢气生成氨气,则B是NH3,D为NO2,二氧化氮和水反应生成硝酸和NO,E能和Cu反应生成NO,则E是HNO3,B→C的方程式为4NH3+5O2
4NO+6H2O,
故答案为:N2;NO2;4NH3+5O2
4NO+6H2O.
| ||
故答案为:S;H2S;SO3;Cu+2H2SO4(浓)
| ||
(2)若A通常状态下为气体单质,根据转化关系知,C是NO,A和氧气反应生成NO,A是N2,氮气和氢气生成氨气,则B是NH3,D为NO2,二氧化氮和水反应生成硝酸和NO,E能和Cu反应生成NO,则E是HNO3,B→C的方程式为4NH3+5O2
| ||
| 高温高压 |
故答案为:N2;NO2;4NH3+5O2
| ||
| 高温高压 |
点评:本题考查无机物的推断,注意A的状态及B能发生连续氧化为解答本题的突破口,熟悉S、N2的单质及化合物的性质是解答的关键,题目难度中等.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
下列关于如图所示有机物的说法中,不正确的是( )
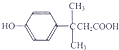

| A、该物质能发生缩聚反应 |
| B、该物质的核磁共振氢谱上共有7个峰 |
| C、该物质能与浓溴水发生反应 |
| D、1mol该物质完全反应最多消耗Na、NaOH、NaHCO3的物质的量之比为2:2:1 |
下列说法中,不正确的是( )
| A、反应热指的是反应过程中吸收或放出的热量 |
| B、原电池的负极发生氧化反应 |
| C、伴随能量变化的不一定是化学变化 |
| D、电解池的阳极发生氧化反应 |
设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A、6.0g金刚石中含有的共价键数为NA |
| B、56g铁粉与酸反应失去的电子数一定为0.2 NA |
| C、1 mol?L-1AlCl3溶液中含有3NA个Cl |
| D、标况下,11.2LSO3所含的分子数为0.5NA |
向NaBr、NaI、Na2SO3混合液中,通入过量氯气后,将溶液蒸干并充分灼烧,得到剩余固体物质的组成是( )
| A、NaCl、NaBr、Na2SO4 |
| B、NaCl、Na2SO4 |
| C、NaCl、Na2SO4、I2 |
| D、NaCl、NaI、Na2SO4 |
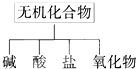 无机化合物可根据其组成和性质进行分类:
无机化合物可根据其组成和性质进行分类:
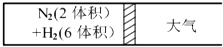 在一定的温度下,把2体积N2和6体积H2分别通入一个带活塞的体积可变的容器中,活塞的一端与大气相通容器中发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0 反应达到平衡后,测得混合气体为7体积.
在一定的温度下,把2体积N2和6体积H2分别通入一个带活塞的体积可变的容器中,活塞的一端与大气相通容器中发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0 反应达到平衡后,测得混合气体为7体积.