题目内容
9.CH2=CHCH=CH2与Br2 按照1:1比例反应,产物可能是( )| A. | CH2=CHCH(Br)CH2Br | B. | CH2=CH(Br)CHCH2Br | C. | CH2=CH2CH2CHBr2 | D. | CH Br2CH=CHCH3 |
分析 CH2=CHCH=CH2为1,3-丁二烯,属于共轭二烯烃,和Br2 按照1:1比例反应时,可以发生1,2-加成,也能发生1,4加成,据此分析.
解答 解:CH2=CHCH=CH2为1,3-丁二烯,属于共轭二烯烃,和Br2 按照1:1比例反应时,可以发生1,2-加成,也能发生1,4加成.
若发生1,2-加成,则产物的结构简式为CH2=CHCH(Br)CH2Br;
若发生1,4-加成,则产物的结构简式为CH2BrCH=CHCH2Br.
故选A.
点评 本题考查有机物结构和性质,为高频考点,明确烯烃发生加成反应特点及位置是解本题关键,侧重考查学生分析判断能力,题目难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
19.通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可以估计化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.下列是一些化学键的键能
根据键能数据估算下列反应的反应热△H为:CH4 (g)+4F2 (g)═CF4(g)+4HF(g)( )
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
| A. | -1940 kJ•mol-1 | B. | 1940 kJ•mol-1 | C. | -485 kJ•mol-1 | D. | 485 kJ•mol-1 |
20.下列实验操作正确的是( )
| A. | 在蔗糖与稀硫酸共热后的溶液中,滴加银氨溶液,验证产物中的葡萄糖 | |
| B. | 淀粉中加入98%的硫酸溶液,在酒精灯上加热,使其水解 | |
| C. | 棉花中加入90%的硫酸,并用玻璃棒把棉花捣烂,在酒精灯上直接加热使其水解 | |
| D. | 向淀粉水解后的溶液中加入碘水,溶液变蓝,证明淀粉尚未水解 |
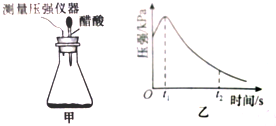
17.某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图甲).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
 (1)上表中编号②实验中铁粉的质量为2.0g;编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响
(1)上表中编号②实验中铁粉的质量为2.0g;编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响
..
(2)编号①试验测得容器中压强随时间变化如图乙.t2时,容器中压强明显小于起始压强,其原因是铁发生了吸氧腐蚀,此时,碳粉表面发生了还原(填“氧化”或“还原”)反应,其电极反应式为O2+2H2O+4e-═4OH-.
(3)该小组对图乙中0~t1时压强增大的原因提出了如下假设:
假设一:发生析氢腐蚀产生了气体
假设二:反应开始时放热,导致容器温度升高,压强增大.
| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验做参照 | 0.5 | 2.0 | 90.0 |
| ② | 探究醋酸浓度的影响 | 0.5 | 36.0 | |
| ③ | 0.2 | 2.0 | 90.0 |
 (1)上表中编号②实验中铁粉的质量为2.0g;编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响
(1)上表中编号②实验中铁粉的质量为2.0g;编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响..
(2)编号①试验测得容器中压强随时间变化如图乙.t2时,容器中压强明显小于起始压强,其原因是铁发生了吸氧腐蚀,此时,碳粉表面发生了还原(填“氧化”或“还原”)反应,其电极反应式为O2+2H2O+4e-═4OH-.
(3)该小组对图乙中0~t1时压强增大的原因提出了如下假设:
假设一:发生析氢腐蚀产生了气体
假设二:反应开始时放热,导致容器温度升高,压强增大.
4.Ⅰ.在发射“神舟”七号的火箭推进器中装有肼(N2H4)和过氧化氢,当两者混合时即产生气体,并放出大量的热.
已知:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641kJ•mol-1
H2O(l)═H2O(g)△H=+44 kJ•mol-1
(1)若用3.2g液态肼与足量过氧化氢反应生成氮气和液态水,则整个过程中转移的电子的物质的量为0.4mol,该反应的热化学方程式为N2H4(l)+2H2O2(l)=N2 (g)+4H2O (l)△H=-817.6 kJ/mol.
(2)肼(N2H4)中N元素的杂化方式是sp3杂化,过氧化氢的电子式为
Ⅱ.某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5,因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
(3)将PM2.5样本用蒸馏水处理制成室温待测试样.
若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断PM2.5待测试样的pH=4.
(4)为减少SO2的排放,常采取的措施有:①将煤转化为清洁气体燃料水煤气.
写出焦炭与水蒸气反应的化学方程式(注明反应条件):C+H2O $\frac{\underline{\;高温\;}}{\;}$CO+H2.
水煤气除可用作燃料气外,请列举一种水煤气的其他用途做还原剂冶炼金属
②洗涤含SO2的烟气.以下物质可作洗涤剂的是bd.
a. Na2SO4 b.Na2CO3 c.CaCl2 d.NaHS.
已知:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641kJ•mol-1
H2O(l)═H2O(g)△H=+44 kJ•mol-1
(1)若用3.2g液态肼与足量过氧化氢反应生成氮气和液态水,则整个过程中转移的电子的物质的量为0.4mol,该反应的热化学方程式为N2H4(l)+2H2O2(l)=N2 (g)+4H2O (l)△H=-817.6 kJ/mol.
(2)肼(N2H4)中N元素的杂化方式是sp3杂化,过氧化氢的电子式为

Ⅱ.某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5,因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
(3)将PM2.5样本用蒸馏水处理制成室温待测试样.
若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(4)为减少SO2的排放,常采取的措施有:①将煤转化为清洁气体燃料水煤气.
写出焦炭与水蒸气反应的化学方程式(注明反应条件):C+H2O $\frac{\underline{\;高温\;}}{\;}$CO+H2.
水煤气除可用作燃料气外,请列举一种水煤气的其他用途做还原剂冶炼金属
②洗涤含SO2的烟气.以下物质可作洗涤剂的是bd.
a. Na2SO4 b.Na2CO3 c.CaCl2 d.NaHS.
14.为了测定某卤代烃分子中所含有的卤原子种类,可按下列步骤进行实验:①量取该卤代烃液体;②冷却后加入稀硝酸酸化;③加入AgNO3溶液至沉淀完全;④加入适量NaOH溶液,煮沸至液体不分层;正确操作顺序为( )
| A. | ④③②① | B. | ①④②③ | C. | ③①④② | D. | ①④③② |
1.下表是元素周期表的一部分,用元素符号或化学式回答下列问题:
(1)最高价氧化物对应的水化物中酸性最强的酸的化学式HClO4,该酸与NaOH溶液反应的离子方程式是:H++OH-=H2O
(2)写出有序号标出的元素中金属性最强的元素在元素周期表中的位置第三周期IA族.
(3)标况下,1mol的①在④中完全燃烧放出285.8kJ热量,写出该反应的热化学方程式2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol.
(4)写出从两种不同角度比较⑥与⑦两种元素金属性的方法根据金属与水或酸反应剧烈程度,比较最高价氧化物对应水化物的碱性强弱.
| 周期 族 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)写出有序号标出的元素中金属性最强的元素在元素周期表中的位置第三周期IA族.
(3)标况下,1mol的①在④中完全燃烧放出285.8kJ热量,写出该反应的热化学方程式2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol.
(4)写出从两种不同角度比较⑥与⑦两种元素金属性的方法根据金属与水或酸反应剧烈程度,比较最高价氧化物对应水化物的碱性强弱.
19.如图表示铁与不同浓度硝酸反应时,各种还原产物的相对含量与硝酸溶液浓度的关系,则下列说法不正确的是( )


| A. | 一般来说,硝酸与铁反应的还原产物不是单一的 | |
| B. | 用一定量的铁粉与大量的9.75mol•L-1HNO3溶液反应得到标态下气体2.24L,则参加反应的硝酸的物质的量为0.1mol. | |
| C. | 硝酸的浓度越大,其还原产物中价态越高的成份越多 | |
| D. | 当硝酸浓度为9.75mol•L-1时还原产物是NO、NO2、N2O,且其物质的量之比为5:3:1 |
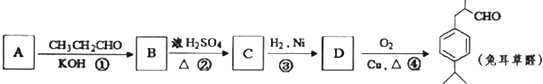
 可写成
可写成
 .
.