题目内容
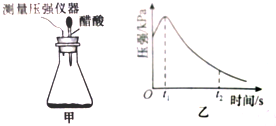
17.某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图甲).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验做参照 | 0.5 | 2.0 | 90.0 |
| ② | 探究醋酸浓度的影响 | 0.5 | 36.0 | |
| ③ | 0.2 | 2.0 | 90.0 |
 (1)上表中编号②实验中铁粉的质量为2.0g;编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响
(1)上表中编号②实验中铁粉的质量为2.0g;编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响..
(2)编号①试验测得容器中压强随时间变化如图乙.t2时,容器中压强明显小于起始压强,其原因是铁发生了吸氧腐蚀,此时,碳粉表面发生了还原(填“氧化”或“还原”)反应,其电极反应式为O2+2H2O+4e-═4OH-.
(3)该小组对图乙中0~t1时压强增大的原因提出了如下假设:
假设一:发生析氢腐蚀产生了气体
假设二:反应开始时放热,导致容器温度升高,压强增大.
分析 (1)根据对比试验中保证变量的唯一性,铁粉质量应该相等,均为2.0g,根据数据可知,编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响;
(2)根据析氢腐蚀与吸氧腐蚀的区别及锥形瓶中压强的变化判断钢铁的腐蚀类型;根据钢铁的腐蚀类型及原理标出电子转移的方向;碳粉表明氧气得到电子生成氢氧根离子,发生还原反应;
(3)图2中0-t1时压强变大,可能是发生了析氢腐蚀使气体体积增大或者反应放热使温度升高,压强增大,锥形瓶中气体体积增大.
解答 解:(1根据对比试验中保证变量的唯一性,铁粉质量应该相等,均为2.0g,根据数据可知,编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响,故答案为:2.0g;探究碳粉的质量对化学反应速率的影响;
(2)t2时,容器中压强明显小于起始压强,说明锥形瓶中气体体积减小,说明发生了吸氧腐蚀,碳为正极,铁为负极,碳电极氧气得到电子发生还原反应,电极反应式为:O2+2H2O+4e-=4OH-,故答案为:吸氧;还原;O2+2H2O+4e-=4OH-;
(3)图2中0-t1时压强变大的原因可能为:铁发生了析氢腐蚀、铁与醋酸的反应为放热反应,温度升高时锥形瓶中压强增大,所以假设二为:反应放热使锥形瓶内温度升高,压强增大,故答案为:反应开始时放热,导致容器温度升高,压强增大.
点评 本题考查了探究铁的腐蚀原理、原电池工作原理,题目难度中等,注意掌握原电池工作原理,明确钢铁的化学腐蚀类型、腐蚀原理及区别.

练习册系列答案
相关题目
7.固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构,则下列有关说法中,不正确的是( )
| A. | 1mol NH5中含有5 mol N-H 键 | |
| B. | NH5的熔沸点高于NH3 | |
| C. | NH5固体投入少量水中,可产生两种气体 | |
| D. | NH5中既有离子键又有共价键 |
8.某化合物的结构(键线式)及球棍模型如下:

该有机分子的核磁共振波谱图如下(单位是ppm).
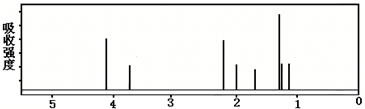
下列关于该有机物的叙述正确的是( )

该有机分子的核磁共振波谱图如下(单位是ppm).

下列关于该有机物的叙述正确的是( )
| A. | 键线式中的Et代表的基团为-CH3 | |
| B. | 该有机物属于芳香族化合物 | |
| C. | 该有机物不同化学环境的氢原子有8种 | |
| D. | 该有机物不可能发生消去反应 |
5.下列说法错误的是( )
| A. | 除氦外的稀有气体原子的最外层电子数都是8 | |
| B. | 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 | |
| C. | 原子及其离子的核外电子层数等于该元素所在的周期数 | |
| D. | 同一元素的各种同位素的化学性质均相同 |
12.下列关于能源的说法错误的是( )
| A. | 煤的干馏包括化学变化和物理变化 | |
| B. | 沼气(主要成分是CH4)是可再生能源 | |
| C. | 人类利用的能源都是通过化学反应获得的 | |
| D. | 石油是由1-50个碳原子的烷烃和环烷烃组成的混合物 |
2.下列说法错误的是( )
| A. | 酒精可以和水以任意比例互溶,与氢键有关 | |
| B. | 邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点,与氢键有关 | |
| C. | 无机含氧酸的化学式可以用XOn(OH)m表示,n值越大,m值越小,则该酸的酸性就越强.则可推知,硫酸酸性强于磷酸 | |
| D. | 两分子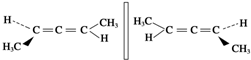 互为手性分子 互为手性分子 |
9.CH2=CHCH=CH2与Br2 按照1:1比例反应,产物可能是( )
| A. | CH2=CHCH(Br)CH2Br | B. | CH2=CH(Br)CHCH2Br | C. | CH2=CH2CH2CHBr2 | D. | CH Br2CH=CHCH3 |
6.化工产品的清洁生产、循环利用、环境友好有利于可持续健康发展.下列举措不合理的是( )
| A. | 用“地沟油”中油脂生产航空生物煤油 | |
| B. | 用细菌浸取法以含硫化铜贫矿制取铜盐 | |
| C. | 用水代替化工合成反应中某些有机 | |
| D. | 将废铅蓄电池深埋处理,节约回收成本 |
7.下列操作或装置能达到实验目的是( )
| A. | 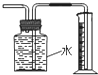 此图装置收集并测量Cu与稀硝酸反应产生的气体及体积 | |
| B. | 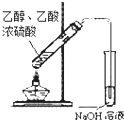 此图装置可用于实验室制取乙酸乙酯 | |
| C. |  检验乙炔的还原性 | |
| D. | 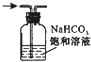 除去氯气中的HCl气体 |