题目内容
设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,1.12LCCl4含有C-Cl键数目为0.2NA | ||
B、标准状况下,2.24L氯气中含有的
| ||
| C、常温常压下,4.4gCO2与N2O混合气体中含有的原子总数为0.3NA | ||
| D、80mL 10mol?L-1 盐酸与足量MnO2加热反应,产生Cl2分子数为0.2NA |
考点:阿伏加德罗常数
专题:
分析:A、标况下,四氯化碳是液态,而气体摩尔体积只适用于气体;
B、氯元素有3517Cl和3717Cl等多种同位素;
C、根据CO2与N2O的摩尔质量均为44g/mol来计算;
D、浓盐酸分别稀盐酸,反应会停止,生成的氯气小于0.2mol.
B、氯元素有3517Cl和3717Cl等多种同位素;
C、根据CO2与N2O的摩尔质量均为44g/mol来计算;
D、浓盐酸分别稀盐酸,反应会停止,生成的氯气小于0.2mol.
解答:
解:A、标况下,四氯化碳是液态,故A错误;
B、自然界中的氯元素有3517Cl和3717Cl等多种同位素,故标况下,2.24L氯气即0.1mol氯气中的
Cl数目一定小于0.2NA,故B错误;
C、CO2与N2O的摩尔质量均为44g/mol,故4.4gCO2与N2O的物质的量为0.1mol,而CO2与N2O均为三原子分子,故0.1mol混合气体中含0.3mol原子,故C正确;
D、浓盐酸的物质的量是0.8mol,完全反应生成氯气0.2mol,由于浓盐酸变成稀盐酸,变化继续反应,故生成的氯气小于0.2mol,故D错误;
故选C.
B、自然界中的氯元素有3517Cl和3717Cl等多种同位素,故标况下,2.24L氯气即0.1mol氯气中的
35 17 |
C、CO2与N2O的摩尔质量均为44g/mol,故4.4gCO2与N2O的物质的量为0.1mol,而CO2与N2O均为三原子分子,故0.1mol混合气体中含0.3mol原子,故C正确;
D、浓盐酸的物质的量是0.8mol,完全反应生成氯气0.2mol,由于浓盐酸变成稀盐酸,变化继续反应,故生成的氯气小于0.2mol,故D错误;
故选C.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
下列说法正确的是( )
| A、CO2溶于水得到的溶液能导电,则CO2属于电解质 |
| B、电解需要通电才能进行 |
| C、氯化氢的水溶液能导电,液态氯化氢不能导电 |
| D、NaCl晶体不能导电,所以NaCl是非电解质 |
下列反应属于放热反应的是( )
| A、焦碳和二氧化碳反应 |
| B、碳和水蒸汽反应 |
| C、碳酸钙高温分解 |
| D、酸碱中和反应 |
含MgCl2、KCl、Na2SO4三种溶质的混合液中,已知其中含Cl-1.5mol,K+和Na+共1.5mol,Mg2+为0.5mol,则SO42-的物质的量为( )
| A、1 mol |
| B、0.5 mol |
| C、0.25 mol |
| D、0.15 mol |
设NA表示阿伏加德罗常数的值,下列有关NA的叙述中正确的是( )
| A、在标准状况下,1 mol O2与1 mol CCl4的体积相同 |
| B、1 mol Na2O2固体中含离子总数为4NA |
| C、在相同条件下,相同体积的CO、N2的混合气体与氢气的分子数、原子数都相同 |
| D、7.1gCl2与5.6gFe反应,转移的电子总数为0.3NA |
下列离子反应方程式中,正确的是( )
| A、铜片插入硝酸银溶液:Cu+Ag+=Cu2++Ag |
| B、在硫酸铜溶液中加入足量氢氧化钡溶液:Ba2++SO42-=BaSO4↓ |
| C、碳酸钠与稀硫酸混合,CO32-+2H+=CO2↑+H2O |
| D、铁溶解于稀盐酸:2Fe+6H+=2Fe3++3H2↑ |
下列有关晶体的说法中正确的是( )
| A、金属晶体和离子晶体都能导电 |
| B、冰、“可燃冰”、干冰都具有分子密堆积特征 |
| C、金属晶体和离子晶体都可采取“紧密堆积”方式,原子晶体都可采取“非紧密堆积”方式 |
| D、金属晶体和离子晶体中分别存在金属键和离子键,很难断裂,都具有延展性 |
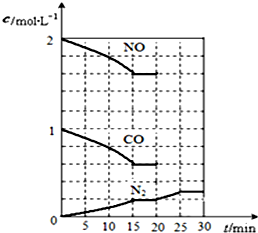 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.