题目内容
下列说法正确的是( )
| A、CO2溶于水得到的溶液能导电,则CO2属于电解质 |
| B、电解需要通电才能进行 |
| C、氯化氢的水溶液能导电,液态氯化氢不能导电 |
| D、NaCl晶体不能导电,所以NaCl是非电解质 |
考点:电解质与非电解质,电解质溶液的导电性
专题:
分析:水溶液中或熔融状态下能够导电的化合物称为电解质,酸、碱、盐都是电解质;在上述两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质.大多数的有机物都是非电解质;单质,混合物不管在水溶液中或熔融状态下能够导电与否,都不是电解质或非电解质.电解是借助电流在阴阳两极引起氧化还原反应的过程.
解答:
解:A、二氧化碳的水溶液导电,电离出自由移动离子的物质是碳酸不是二氧化碳,所以二氧化碳是非电解质,故A错误;
B、电解是借助电流在阴阳两极引起氧化还原反应的过程,故电解必须通电才能进行,故B正确;
C、氯化氢的水溶液能导电,所以液态氯化氢是电解质,故C正确;
D、氯化钠晶体没有自由移动的离子,所以不导电,但氯化钠的水溶液能导电,所以氯化钠是电解质,故D错误.
故选BC.
B、电解是借助电流在阴阳两极引起氧化还原反应的过程,故电解必须通电才能进行,故B正确;
C、氯化氢的水溶液能导电,所以液态氯化氢是电解质,故C正确;
D、氯化钠晶体没有自由移动的离子,所以不导电,但氯化钠的水溶液能导电,所以氯化钠是电解质,故D错误.
故选BC.
点评:本题考查了电解质和非电解质的判断及电解的概念,难度不大,易错题是A,注意能导电的不一定是电解质,如金属;电解质不一定导电,如氯化钠固体,注意电解与电离的不同.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
下列有关物质性质的应用正确的是( )
| A、氯化钠溶液显中性,可用铝制容器贮存氯化钠溶液 |
| B、碳酸钠溶液显碱性,可用热的纯碱溶液除去金属器件表面油污 |
| C、氮气化学性质通常不活泼,可将炽热的镁粉可放在氮气中冷却 |
| D、铜的金属性比铁弱,可将海轮浸水部分镶上铜锭以减缓船体腐蚀 |
在强酸性溶液中,可以大量共存的离子组是( )
| A、Al3+、Na+、SO42- |
| B、K+、NO3-、CO32- |
| C、Na+、HCO3-、Cl- |
| D、Ag+、Al3+、Cl- |
为了检验SO42-,甲、乙、丙、丁四位同学设计了如下4种方案,其中方案最优的是( )
A、方案甲:试液
| ||||
B、方案乙:试液
| ||||
C、方案丙:试液
| ||||
D、方案丁:试液
|
化学无处不在,下列与化学有关的说法不正确的是( )
| A、可用蘸浓硫酸的棉花棒检验输送氨气的管道是否漏气 |
| B、“地沟油”禁止食用,但可用来制肥皂 |
| C、从海水中提取物质都必须经过化学反应才能实现 |
| D、侯式制碱法的工艺过程中应用了物质溶液度的差异 |
关于如图所示装置的判断,叙述正确的是( )
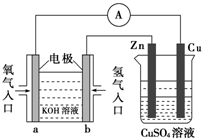

| A、左边的装置是电解池,右边的装置是原电池 |
| B、该装置中铜为正极,锌为负极 |
| C、当铜片的质量变化为12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L |
| D、装置中电子的流向是:a→Cu→经过CuSO4溶液→Zn→b |
设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,1.12LCCl4含有C-Cl键数目为0.2NA | ||
B、标准状况下,2.24L氯气中含有的
| ||
| C、常温常压下,4.4gCO2与N2O混合气体中含有的原子总数为0.3NA | ||
| D、80mL 10mol?L-1 盐酸与足量MnO2加热反应,产生Cl2分子数为0.2NA |