题目内容
下列说法中错误的是( )
| A、从2L1mol?L-1的NaCl溶液中取出10 mL,其浓度仍是1 mol?L-1 |
| B、制成0.5L 1 mol?L-1的盐酸,需标准状况下氯化氢气体11.2 L |
| C、1L1mol?L-1 BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 |
| D、10g98%硫酸(密度为1.84g?cm-3)与10mL 18.4 mol?L-1硫酸的浓度是不同的 |
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:A、根据溶液为均一、稳定的混合物来分析;
B、根据n=c?v计算出氯化氢的物质的量,再根据V=n?Vm来计算标况下需要氯化氢的体积;
C、根据n=c?v计算出溶质氯化钡的物质的量,再根据N=n?NA来计算钡离子和氯离子的数目;
D、据c=
计算出浓硫酸的物质的量浓度,然后进行判断.
B、根据n=c?v计算出氯化氢的物质的量,再根据V=n?Vm来计算标况下需要氯化氢的体积;
C、根据n=c?v计算出溶质氯化钡的物质的量,再根据N=n?NA来计算钡离子和氯离子的数目;
D、据c=
| 1000ρω |
| M |
解答:
解:A、溶液为均一、稳定的混合物,从2L 1mol?L-1的NaCl溶液中取出10mL,浓度不变,浓度仍是1mol?L-1,故A正确;
B、制成0.5L 1mol?L-1的盐酸,需要氯化氢的物质的量为:n(HCl)=c?v=0.5L×1mol?L-1=0.5mol,标准状况下氯化氢的体积为:V(HCl)=n?Vm=0.5mol×22.4mol?L-1=11.2L,故B正确;
C、1L 1mol?L-1 BaCl2溶液中,n(BaCl2)=c?v=1L×1mol?L-1=1mol,由BaCl2的构成可知,1molBaCl2含2mol氯离子、1mol钡离子,Ba2+和Cl-总数为:3×6.02×1023,故C正确;
D、据c=
可知,98%硫酸(密度为1.84g?cm-3)的物质的量浓度为:c=
mol/L=18.4mol?L-1,与10mL 18.4 mol?L-1硫酸的浓度是相同的,故D错误;
故选D.
B、制成0.5L 1mol?L-1的盐酸,需要氯化氢的物质的量为:n(HCl)=c?v=0.5L×1mol?L-1=0.5mol,标准状况下氯化氢的体积为:V(HCl)=n?Vm=0.5mol×22.4mol?L-1=11.2L,故B正确;
C、1L 1mol?L-1 BaCl2溶液中,n(BaCl2)=c?v=1L×1mol?L-1=1mol,由BaCl2的构成可知,1molBaCl2含2mol氯离子、1mol钡离子,Ba2+和Cl-总数为:3×6.02×1023,故C正确;
D、据c=
| 1000ρω |
| M |
| 1000×1.84×98% |
| 98 |
故选D.
点评:本题考查物质的量浓度的理解、计算,题目难度中等,试题侧重基础知识的考查,注意掌握物质的量浓度、溶质质量分数的概念及计算方法,明确二者之间的转化关系.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
铝制器皿能够盛放的物质是( )
| A、KOH溶液 | B、NaOH溶液 |
| C、浓硫酸 | D、稀硝酸 |
下列有关氧化还原反应的说法正确的是( )
| A、2Na2O2+2H2O=4NaOH+O2↑ 反应中,Na2O2是氧化剂,H2O是还原剂 |
| B、CaH2+2H2O=Ca(OH)2+2H2↑ 反应中,Ca(OH)2既不是氧化产物也不是还原产物 |
| C、KClO3+6HCl=KCl+3Cl2↑+3H2O 反应中,转移的电子数为6e- |
| D、KClO3+6HCl=KCl+3Cl2↑+3H2O 反应中,被氧化的氯元素与被还原的氯元素质量比为6:1 |
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA |
| B、在非标准状况下,1mol任何气体的体积不可能是22.4L |
| C、标准状况下,22.4L酒精(CH3CH2OH)的分子数为NA |
| D、一定条件下,2.3g的Na完全与O2反应失去的电子数为0.1NA |
下列说法不正确的是( )
| A、要想使AlCl3溶液中的Al3+几乎全部沉淀出来,可以加入过量的氨水 |
| B、向FeCl2溶液中加入氨水,最终会看到红褐色沉淀 |
| C、保存硫酸亚铁溶液时常在其中加颗铁钉 |
| D、氢氧化钠、纯碱溶液要存放在带磨砂玻璃塞的试剂瓶中 |
关于氢键,下列说法正确的是( )
| A、氢键属于共价键 |
B、因为分子间存在氢键的缘故,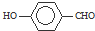 比 比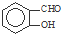 熔沸点高 熔沸点高 |
| C、由于氢键比范德华力强,所以H2O分子比H2S分子稳定 |
| D、1mol冰中有4mol氢键 |
下列离子方程式书写正确的是( )
| A、向氯化铝溶液中加入过量的氨水:3NH3?H2O+A13+═3NH4++Al(OH)3↓ |
| B、NaOH溶液吸收少量CO2:OH-+CO2═HCO3- |
| C、向氯化铁溶液中加入铜粉发生的反应:Cu+Fe3+═Cu2++Fe2+ |
| D、Na2O2与水的反应:Na2O2+H2O═2Na++2OH-+O2 |