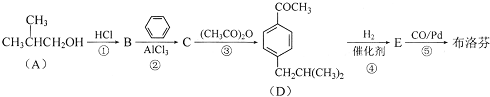
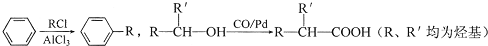题目内容
容积完全相同的两个容器甲和乙,已知甲中装有SO2、O2各1mol,乙中装有SO2、O2各2mol,在同一温度下反应,2SO2(g)+O2(g)?2SO3(g)达平衡时,下列比较不正确的是( )
| A、反应速率:甲<乙 |
| B、O2浓度:甲<乙 |
| C、O2的转化率:甲<乙 |
| D、SO2的百分含量:甲<乙 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:体积相等时,甲中装有SO2、O2各1mol,乙中装有SO2、O2各2mol,相同温度下,将乙体积扩大为甲的二倍,这时二者为等效平衡,乙达到平衡状态时体积缩小到和原来体积相等,相当于增大压强,平衡向正反应方向移动,据此分析解答.
解答:
解:体积相等时,甲中装有SO2、O2各1mol,乙中装有SO2、O2各2mol,相同温度下,将乙体积扩大为甲的二倍,这时二者为等效平衡,乙达到平衡状态时体积缩小到和原来体积相等,相当于增大压强,平衡向正反应方向移动,
A.反应物浓度越大,反应速率越大,乙中反应物浓度大于甲,则反应速率甲<乙,故A正确;
B.等效平衡时甲乙中氧气转化率相等,乙达到平衡时,然后缩小容器体积和甲相等,乙中氧气的转化率大于甲,但转化的氧气量较少,所以氧气浓度甲<乙,故B正确;
C.根据以上分析知,氧气的转化率甲小于乙,故C正确;
D.达到平衡状态时,氧气的转化率甲<乙,所以SO2的百分含量:甲>乙,故D错误;
故选D.
A.反应物浓度越大,反应速率越大,乙中反应物浓度大于甲,则反应速率甲<乙,故A正确;
B.等效平衡时甲乙中氧气转化率相等,乙达到平衡时,然后缩小容器体积和甲相等,乙中氧气的转化率大于甲,但转化的氧气量较少,所以氧气浓度甲<乙,故B正确;
C.根据以上分析知,氧气的转化率甲小于乙,故C正确;
D.达到平衡状态时,氧气的转化率甲<乙,所以SO2的百分含量:甲>乙,故D错误;
故选D.
点评:本题考查化学平衡,侧重考查分析计算能力,正确构建等效平衡是解本题关键,然后利用外界条件对化学平衡影响分析,题目难度中等.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
我国国家药品监督管理局在2000年11月16日发出紧急通知,立即禁止使用含有PPA的抗感冒药物.PPA是盐酸苯丙醇胺的英文缩写,已知苯丙醇胺的结构简式如图所示,下列对苯丙醇胺叙述错误的是( )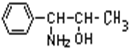
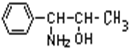
| A、一定条件下,可以发生消去反应 |
| B、一定条件下与Br2可以发生苯环上的取代反应 |
| C、具有弱碱性,可与强酸反应生成盐 |
| D、具有弱酸性,可与强碱反应生成盐 |
用四氯化碳萃取溴水中的溴,下列说法中不正确的是( )
| A、实验中使用的主要仪器是分液漏斗 |
| B、溴在四氯化碳中的溶解度比在水中的溶解度大 |
| C、不可把萃取剂四氯化碳换成酒精 |
| D、分液时,水从分液漏斗下口流出,溴的四氯化碳溶液从分液漏斗上口倒出 |
下列各组元素都属于p区的是( )
| A、原子序数为1,6,7的元素 |
| B、He,S,P |
| C、Fe,Cu,Cl |
| D、Na,Li,Mg |
下列各组物质中,第一种是酸,第二种是混合物,第三种是碱的是.
| A、硫酸、CuSO4?5H2O、纯碱 |
| B、硫酸氢钠、空气、纯碱 |
| C、氧化铁、明矾、熟石灰 |
| D、硝酸、食盐水、烧碱 |
把NaHCO3和Na2CO3?10H2O混合物6.56g溶于水配成100mL溶液,c(Na+)=0.5mol/L.如将溶液蒸干、灼烧,所得固体为(2NaHCO3=Na2CO3+H2O+CO2↑条件:加热)( )
| A、2.65 g |
| B、2.96 g |
| C、6.56g |
| D、5.3g |
根据热化学方程式S(g)+O2═SO2(g);△H=-297.23kJ/mol下列说法中正确的是( )
| A、S(g)+O2═SO2(1);|△H|>297.3kJ/mol |
| B、S(g)+O2═SO2(1);|△H|<297.3kJ/mol |
| C、1molSO2的键能总和小于1molS和1molO2键能之和 |
| D、1molSO2的键能总和等于1molS和1molO2键能之和 |
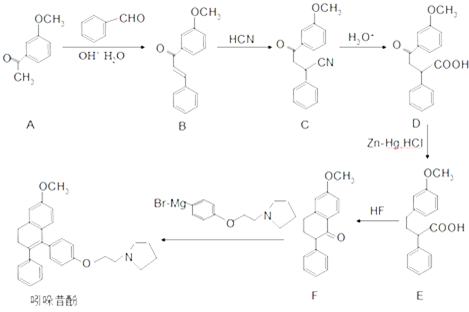
 ]是有机合成中间体,请设计合理的方案以丙酮
]是有机合成中间体,请设计合理的方案以丙酮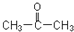 )为唯一有机原料合成2,2-二甲基戊酸(用合成路线流程图表示,并注明反应条件).提示:①合成过程中无机试剂任选;
)为唯一有机原料合成2,2-二甲基戊酸(用合成路线流程图表示,并注明反应条件).提示:①合成过程中无机试剂任选;