��Ŀ����
16��������ˮ��D2O����������D2O�����ӻ���1.6��10-15���������ú�pHֵһ���Ķ������涨�������ӵĸ�����pD�����й���pDֵ��������ȷ���ǣ�������| A�� | ������ˮ��pDֵΪ7 | |
| B�� | ��1L��ˮ���ܽ�0.01molDCl����pDֵΪ4 | |
| C�� | ��1L��ˮ���ܽ�0.01mol NaOD����pDֵΪ12 | |
| D�� | ��100mL 0.25mol/L��DCl��ˮ��Һ�м���50mL0.2mol/L��NaOD����ˮ��Һʱ����pDֵΪ1 |
���� A������pD=-lg[D+]���㣻
B������pD=-lg[D+]���㣻
C���ȼ���NaODŨ�ȣ��ٸ������ӻ���������D+Ũ�ȣ�
D�������n��DC����n��NaOD�������ʵ������жϷ�Ӧ����Һ����ԣ��ڽ���������Һ��pD��
��� �⣺A��c��D+��=$\sqrt{1.6��1{0}^{-15}}$mol/L=4��10-8mol/L������pD��7����A����
B��c��DC1��=$\frac{0.01mol}{1L}$=0.01mol/L����c��D+��=0.01mol/L������pD=2����B����
C��c��NaOD��=$\frac{0.01mol}{1L}$=0.01mol/L����c��D+��=$\frac{1.6��1{0}^{-15}}{0.01}$=1.6��10-13mol/L����pD��12����C����
D��n��DCl��=0.025mol��n��NaOD��=0.01mol��D+��ʣ�࣬ʣ���n��D+��=0.015mol����Ӧ����Һ�У�c��D+��=0.015��0.15L=0.1mol/L����pD=1.0����D��ȷ��
��ѡD��
���� ���⿼��pH�ļ��㣬������Һ��Ũ�Ƚ�����ӻ���������ɣ��ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
4����ʹƽ��H2O?H++OH-�������ƶ�����ʹ��Һ�����Եķ����ǣ�������
| A�� | ��ˮ�м����������������ƹ��� | B�� | ��ˮ�м�����������ˮ����ͭ���� | ||
| C�� | ��ˮ�м���������̼���ƹ��� | D�� | ��ˮ���ȵ�95�棬ʹˮ��pH=6 |
11������34.6g ��CuCO3��Cu2��OH��2CO3��ɵĻ�������300mL 2mol•L-l������ǡ����ȫ��Ӧ�������ȷֽ�����������ֻ����ɵ�Cu0��������Ϊ��������
| A�� | 16.0g | B�� | 19.2g | C�� | 24��Og | D�� | 30.6g |
8������˵���У��ڿ�ѧ��û�д�����ǣ�������
| A�� | ��������������̣��������� | |
| B�� | �˹��ϳɵľ����������Եĵ�����-�ᾧţ�ȵ��أ���1965���ҹ���ѧ�����Ⱥϳɵ� | |
| C�� | ����Ȼ������ɵ����ϣ������κλ�ѧ���� | |
| D�� | ����ˮ���Դ��������в����κη��� |
5��ij��������Һ�У������������ܴ���������ǣ�������
| A�� | K+��H+��SO42-��OH- | B�� | Na+��Ba2+��CO32-��NO3- | ||
| C�� | Na+��H+��Cl-��NO3- | D�� | Mg2+��Cu2+��Cl-��SO42- |
3����һ��������ܱ������У��������»�ѧ��Ӧ��
CO2��g��+H2��g��?CO��g��+H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=$\frac{c��CO��•c��{H}_{2}O��}{c��C{O}_{2}��•c��{H}_{2}��}$���÷�ӦΪ���ȷ�Ӧ��ѡ����ȡ��������ȡ�����
��2�����жϸ÷�Ӧ�Ƿ��Ѵﻯѧƽ��״̬��������bc��
a��������ѹǿ����b�����������c��CO������
c��v����H2��=v�棨H2O��d��c��CO2��=c��CO��
��3��830��ʱ�������еķ�Ӧ�Ѵﵽƽ�⣮�������������������£����������������ƽ�ⲻ�ƶ���ѡ�������Ӧ���������淴Ӧ��������������
��4���� 830��ʱ���������г���1mol CO��5mol H2O����Ӧ�ﵽƽ����仯ѧƽ�ⳣ��K����1.0��ѡ����ڡ�����С�ڡ��������ڡ���
��5����1200��ʱ����ijʱ��ƽ����ϵ��CO2��H2��CO��H2O��Ũ�ȷֱ�Ϊ2mol•L-1��2mol•L-1��4mol•L-1��4mol•L-1�����ʱ������Ӧ��ƽ���ƶ�����Ϊ�淴Ӧ����ѡ�����Ӧ�������淴Ӧ���������ƶ�����
��6��ij�¶��£���2L���ܱ������У�����1molCO2��1molH2��ַ�Ӧ��ƽ��ʱ��COƽ��Ũ��Ϊ0.25mol/L�����жϴ�ʱ���¶�Ϊ830�森
��7�����ڣ�6���������¶��£���1L���ܱ������У�����2molCO2��3molH2��ַ�Ӧ��ƽ��ʱ��H2�����ʵ���Ϊb��
a������1.0mol��������b������1.0molc������0.5mold����ȷ����
CO2��g��+H2��g��?CO��g��+H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
��2�����жϸ÷�Ӧ�Ƿ��Ѵﻯѧƽ��״̬��������bc��
a��������ѹǿ����b�����������c��CO������
c��v����H2��=v�棨H2O��d��c��CO2��=c��CO��
��3��830��ʱ�������еķ�Ӧ�Ѵﵽƽ�⣮�������������������£����������������ƽ�ⲻ�ƶ���ѡ�������Ӧ���������淴Ӧ��������������
��4���� 830��ʱ���������г���1mol CO��5mol H2O����Ӧ�ﵽƽ����仯ѧƽ�ⳣ��K����1.0��ѡ����ڡ�����С�ڡ��������ڡ���
��5����1200��ʱ����ijʱ��ƽ����ϵ��CO2��H2��CO��H2O��Ũ�ȷֱ�Ϊ2mol•L-1��2mol•L-1��4mol•L-1��4mol•L-1�����ʱ������Ӧ��ƽ���ƶ�����Ϊ�淴Ӧ����ѡ�����Ӧ�������淴Ӧ���������ƶ�����
��6��ij�¶��£���2L���ܱ������У�����1molCO2��1molH2��ַ�Ӧ��ƽ��ʱ��COƽ��Ũ��Ϊ0.25mol/L�����жϴ�ʱ���¶�Ϊ830�森
��7�����ڣ�6���������¶��£���1L���ܱ������У�����2molCO2��3molH2��ַ�Ӧ��ƽ��ʱ��H2�����ʵ���Ϊb��
a������1.0mol��������b������1.0molc������0.5mold����ȷ����
 ��
�� ��
��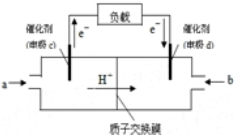 ���ſ�ѧ�����Ľ��������������˶��ּ״����ӽ���Ĥȼ�ϵ�أ������㲻ͬ������
���ſ�ѧ�����Ľ��������������˶��ּ״����ӽ���Ĥȼ�ϵ�أ������㲻ͬ������