题目内容
11.现有34.6g 由CuCO3和Cu2(OH)2CO3组成的混合物,可与300mL 2mol•L-l的盐酸恰好完全反应;若加热分解等质量的这种混合物可得Cu0固体质量为( )| A. | 16.0g | B. | 19.2g | C. | 24.Og | D. | 30.6g |
分析 CuCO3 和Cu2(OH)2CO3的混合物和盐酸反应生成CuCl2,加热分解生成CuO,根据消耗盐酸的物质的量结合质量守恒定律计算CuO的物质的量、质量.
解答 解:CuCO3和Cu2(OH)2CO3与盐酸反应的关系式为:CuCO3$\stackrel{HCl}{→}$CuCl2,Cu2(OH)2CO3$\stackrel{HCl}{→}$2CuCl2,
300mL 2mol•L-l的盐酸中含有HCl的物质的量为:n(HCl)=0.3L×2mol•L-1=0.6mol,
则n(CuCl2)=$\frac{1}{2}$×n(HCl)=$\frac{1}{2}$×0.6mol=0.3mol,
又有:Cu2(OH)2CO3→2CuO,Cu(OH)2→CuO,
根据Cu元素质量守恒,则:n(CuO)=n(CuCl2)=0.3mol,
则m(CuO)=0.3mol×80g/mol=24.0g,
故选C.
点评 本题考查混合物反应的计算,题目难度不大,本题注意根据Cu元素质量守恒的角度解答,正确书写反应的关系式为解答本题的关键.

练习册系列答案
相关题目
2.除去如表物质中的杂质(括号内为杂质,所选用的试剂及操作方法均正确的一组是( )
| 选项 | 被提纯的物质 | 选用试剂 | 操作方法 |
| A | CaO(CaCO3) | 水 | 溶解、过滤、结晶 |
| B | CuSO4(H2SO4) | NaOH溶液 | 过滤 |
| C | CO2(CO) | 氧气 | 点燃 |
| D | Cu(CuO) | 稀盐酸 | 溶解、过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
19.向纯水中加入下列物质,对水的电离平衡几乎没有影响的是( )
| A. | 硫酸钠 | B. | 氨水 | C. | 醋酸 | D. | 盐酸 |
16.对于重水(D2O)(常温下D2O的离子积是1.6×10-15),可以用和pH值一样的定义来规定重氢离子的负对数pD,下列关于pD值的叙述正确的是( )
| A. | 中性重水的pD值为7 | |
| B. | 在1L重水中溶解0.01molDCl,其pD值为4 | |
| C. | 在1L重水中溶解0.01mol NaOD,其pD值为12 | |
| D. | 在100mL 0.25mol/L的DCl重水溶液中加入50mL0.2mol/L的NaOD的重水溶液时,其pD值为1 |
3.在恒温条件下,能使 A(g)+B(g)?C(g)+D(g)正反应速率增大的措施是( )
| A. | 减小C 或D 的浓度 | B. | 增大压强 | ||
| C. | 减小B 的浓度 | D. | 增大 A 或B的浓度 |
18.向某无色透明溶液中加入铝粉,能放出氢气,则此溶液中可能大量共存的离子组是( )
| A. | HSO4-、Na+、OH-、K+ | B. | HCO3-、NO3-、Mg2+、Ba2+ | ||
| C. | Ba2+、Mg2+、NO3-、Cl- | D. | Mg2+、Na+、Cl-、SO42- |
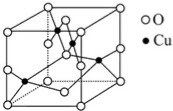 太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、锎、硼、镓、硒等.回答下列问題:
太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、锎、硼、镓、硒等.回答下列问題: 呵护生存环境,共建和谐社会.
呵护生存环境,共建和谐社会.