题目内容
已知铁的相对原子质量为56,则1个铁原子的质量是 g.
考点:物质的量的相关计算
专题:计算题
分析:铁的相对原子质量为56,则其摩尔质量为56g/mol,故1molFe原子质量为56g,结合1molFe含有6.02×10-23个Fe原子计算.
解答:
解:铁的相对原子质量为56,则其摩尔质量为56g/mol,故1molFe原子质量为56g,而1molFe含有6.02×10-23个Fe原子,故1个铁原子的质量是
=9.3×10-23g,故答案为:9.3×10-23.
| 56g |
| 6.02×1023 |
点评:本题考查摩尔质量、阿伏伽德罗常数,比较基础,侧重对基础知识的巩固.

练习册系列答案
相关题目
将铁片和银片用导线连接置于同一稀盐酸中,经过一段时间后,下列叙述正确的是( )
| A、负极有Cl2逸出,正极有H2逸出 |
| B、负极附近Cl-的浓度逐渐减小 |
| C、正极附近Cl-的浓度逐渐增大 |
| D、溶液中Cl-的浓度基本不变 |
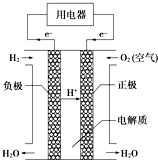 上海世博会有千辆氢氧燃料电池车上路,参看某种氢氧燃料电池原理图,下列说法不正确的是( )
上海世博会有千辆氢氧燃料电池车上路,参看某种氢氧燃料电池原理图,下列说法不正确的是( )| A、氢氧燃料电池是一种具有应用前景的绿色电源 |
| B、氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
| C、氢氧燃料电池能量转换率比氢气直接燃烧高 |
| D、氢氧燃料电池工作时,发出淡蓝色火焰 |
 已知NaCl晶体的晶胞如图所示,它向三维空间延伸得到完美晶体.NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的核间距离为a×10-8cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7g?mol-1).
已知NaCl晶体的晶胞如图所示,它向三维空间延伸得到完美晶体.NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的核间距离为a×10-8cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7g?mol-1).
 →
→