题目内容
某氯化钾样品中含少量杂质硫酸钾和碳酸钾,为了除去杂质,要做以下实验:
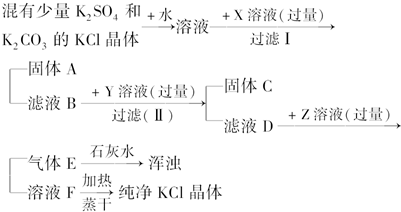
试根据上述实验方案回答:
(1)气体E是 ,X ,Y .
(2)固体A的成分 ,固体C的成分 .(填化学式)

试根据上述实验方案回答:
(1)气体E是
(2)固体A的成分
考点:物质分离、提纯的实验方案设计
专题:实验设计题
分析:氯化钾样品中含少量杂质硫酸钾和碳酸钾,样品溶于水配成溶液,溶液中含有KCl、K2CO3、K2SO4,向溶液中加入过量X BaCl2溶液,发生反应CO32-+Ba2+=BaCO3↓、SO42-+Ba2+=BaSO4↓,得到固体A为:BaCO3和BaSO4的混合物,滤液B中含有KCl、BaCl2,向滤液中加入过量Y K2CO3,除去过量的Ba2+,得到固体C为BaCO3,D中溶质为K2CO3和KCl,然后向溶液中加入过量Z HCl溶液,反应的离子方程式为:CO32-+2H+=H2O+CO2↑,然后蒸发溶液,溶液中HCl挥发,最终得到KCl晶体,据此进行解答.
解答:
解:样品溶于水配制的溶液中含有KCl、K2CO3、K2SO4,其中CO32-、SO42-为杂质,先加入过量的X BaCl2溶液,除去碳酸根离子和硫酸根离子,反应方程式为:CO32-+Ba2+=BaCO3↓、SO42-+Ba2+=BaSO4↓,得到固体A为:BaCO3、BaSO4,滤液B中含有KCl、过量的BaCl2,向滤液中加入过量Y K2CO3溶液,除去过量的Ba2+离子,得到固体C为BaCO3,D中溶质为K2CO3和KCl,然后向溶液中加入过量Z HCl溶液,除去杂质碳酸根离子,发生反应:CO32-+2H+=H2O+CO2↑,则气体E为CO2,然后蒸发溶液,溶液中HCl挥发,最终可得到KCl晶体,
(1)根据以上分析可知,气体E为CO2,X为BaCl2溶液,Y为K2CO3溶液,故答案为:CO2;BaCl2;K2CO3;
(2)固体A的成分为BaCO3和BaSO4的混合物,固体C为BaCO3,故答案为:BaCO3和BaSO4;BaCO3.
(1)根据以上分析可知,气体E为CO2,X为BaCl2溶液,Y为K2CO3溶液,故答案为:CO2;BaCl2;K2CO3;
(2)固体A的成分为BaCO3和BaSO4的混合物,固体C为BaCO3,故答案为:BaCO3和BaSO4;BaCO3.
点评:本题以混合物的分离和提纯为载体考查了无机物推断,题目难度中等,明确物质的性质是解本题关键,根据物质之间的反应、物质分离和提纯的方法等知识点来分析解答,难点是除杂剂的选取及滴加顺序.

练习册系列答案
相关题目
下列物质中既能与盐酸又能与氢氧化钠溶液反应的是( )
| A、CuO |
| B、Na2CO3 |
| C、Fe2O3 |
| D、Al(OH)3 |
下列有关化学用语使用正确的是( )
| A、乙酸、葡萄糖、淀粉的最简式均为CH2O |
B、醛基的电子式: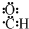 |
C、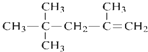 的名称为:2,4,4-三甲基-1-戊烯 的名称为:2,4,4-三甲基-1-戊烯 |
D、乙醇分子比例模型: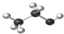 |
下列说法正确的是( )
| A、200ml 1 mol/L Al2(SO4)3溶液中,Al3+和SO42-离子总数为6.02×1023 |
| B、标准状况下11.2L氦气中含有的原子个数为1NA |
| C、46g NO2和N2O4的混合物含有的原子数为3NA |
| D、标准状况下,11.2L苯所含的分子数为0.5 NA |
若要配制250mL溶液,应选用的容量精密的仪器的是( )
| A、500L的容量瓶 |
| B、250mL的烧杯 |
| C、250mL的容量瓶 |
| D、250mL的量筒 |