题目内容
写出下列反应的离子方程式:
(1)钠投入到水中反应的离子方程式为:
(2)服用胃舒平[主要成分是Al(OH)3]治疗胃溃疡,反应的离子方程式为:
(3)铁片插入硫酸铜溶液中: .
(4)CH3COOH与NaOH溶液的中和反应:
(5)Ba(OH)2与CuSO4溶液反应: .
(1)钠投入到水中反应的离子方程式为:
(2)服用胃舒平[主要成分是Al(OH)3]治疗胃溃疡,反应的离子方程式为:
(3)铁片插入硫酸铜溶液中:
(4)CH3COOH与NaOH溶液的中和反应:
(5)Ba(OH)2与CuSO4溶液反应:
考点:离子方程式的书写
专题:离子反应专题
分析:(1)钠与水反应生成氢氧化钠和氢气;
(2)氢氧化铝与盐酸反应生成氯化铝和水;
(3)铁与硫酸铜反应生成硫酸亚铁和铜;
(4)CH3COOH与NaOH溶液的中和反应,生成醋酸钠和水;
(5)Ba(OH)2与CuSO4溶液反应,生成硫酸钡和氢氧化铜.
(2)氢氧化铝与盐酸反应生成氯化铝和水;
(3)铁与硫酸铜反应生成硫酸亚铁和铜;
(4)CH3COOH与NaOH溶液的中和反应,生成醋酸钠和水;
(5)Ba(OH)2与CuSO4溶液反应,生成硫酸钡和氢氧化铜.
解答:
解:(1)钠与水反应生成氢氧化钠和氢气,离子方程式:2Na+2H2O═2Na++2OH-+H2↑;
故答案为:2Na+2H2O═2Na++2OH-+H2↑;
(2)氢氧化铝与盐酸反应生成氯化铝和水,离子方程式为:Al(OH)3+3H+═Al3++3H2O;
故答案为:Al(OH)3+3H+═Al3++3H2O;
(3)铁片插入硫酸铜溶液中,离子方程式为:Fe+Cu2+=Fe2++Cu;
故答案为:Fe+Cu2+=Fe2++Cu;
(4)CH3COOH与NaOH溶液的中和反应,离子方程式为:CH3COOH+OH-═CH3COO-+H2O;
故答案为:CH3COOH+OH-═CH3COO-+H2O;
(5)Ba(OH)2与CuSO4溶液反应,生成硫酸钡和氢氧化铜,离子方程式为:Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓;
故答案为:Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓.
故答案为:2Na+2H2O═2Na++2OH-+H2↑;
(2)氢氧化铝与盐酸反应生成氯化铝和水,离子方程式为:Al(OH)3+3H+═Al3++3H2O;
故答案为:Al(OH)3+3H+═Al3++3H2O;
(3)铁片插入硫酸铜溶液中,离子方程式为:Fe+Cu2+=Fe2++Cu;
故答案为:Fe+Cu2+=Fe2++Cu;
(4)CH3COOH与NaOH溶液的中和反应,离子方程式为:CH3COOH+OH-═CH3COO-+H2O;
故答案为:CH3COOH+OH-═CH3COO-+H2O;
(5)Ba(OH)2与CuSO4溶液反应,生成硫酸钡和氢氧化铜,离子方程式为:Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓;
故答案为:Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓.
点评:本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,注意电荷守恒及在离子反应中应保留化学式的物质,题目难度不大.

练习册系列答案
相关题目
某溶液中有Fe3+、Mg2+、Fe2+和Na+四种离子,若向其中加入过量的NaOH溶液,微热并搅拌,再加入过量盐酸,溶液中大量增加的阳离子是( )
| A、Fe3+ |
| B、Mg2+ |
| C、Na+ |
| D、Fe2+ |
下列对于某些离子的检验说法中正确的是( )
| A、加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- |
| B、某溶液与NaOH溶液共热,产生使湿润蓝色石蕊试纸变红气体,说明原溶液中存在NH4+ |
| C、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| D、可用焰色反应实验检验溶液中是否含有K+ |
下列操作中,一定不需要加热的是( )
| A、萃取 | B、蒸馏 | C、蒸发 | D、溶解 |
鉴别NaOH、Na2CO3、Ba(OH)2三种溶液,最好选用下列试剂中的( )
| A、石蕊溶液 |
| B、稀盐酸 |
| C、稀硫酸 |
| D、CaCl2溶液 |
某温度下,在一容积可变的密闭容器里,反应2A(g)?B(g)+2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol、4mol.在保持温度和压强不变的条件下,下列说法正确的是( )
| A、充入1mol稀有气体氦(He),平衡将向正反应方向移动 |
| B、充入A、B、C各1mol,平衡将向正反应方向移动 |
| C、将A、B、C各物质的量都减半,C的百分含量变大 |
| D、加入一定量的A气体达平衡后,C的百分含量一定增加 |

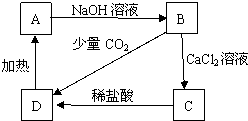 A、B、C、D均为含硅的化合物,其中B的水溶液俗称水玻璃,其相互转化关系如图所示.
A、B、C、D均为含硅的化合物,其中B的水溶液俗称水玻璃,其相互转化关系如图所示.