题目内容
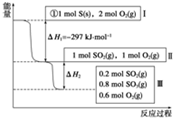 恒温,容积为1L恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示(已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1),请回答下列问题:
恒温,容积为1L恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示(已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1),请回答下列问题:(1)写出能表示硫的燃烧热的热化学方程式:
(2)△H2=
考点:反应热和焓变
专题:化学反应中的能量变化
分析:(1)燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物放出的热量;
(2)根据热化学方程式:2SO2(g)+O2(g)?2SO3(g)△H=-196.6KJ?mol-1计算.
(2)根据热化学方程式:2SO2(g)+O2(g)?2SO3(g)△H=-196.6KJ?mol-1计算.
解答:
解:(1)燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物放出的热量,所以,硫的物质的量为1mol.由图1可知1molS(s)完全燃烧放出的热量为297KJ,所以,硫的燃烧热的热化学方程式S(s)+O2(g)═SO2(g)△H=-297 KJ?mol-1,
故答案为:S(s)+O2(g)═SO2(g)△H=-297 KJ?mol-1;
(2)由由图1可知,参加反应的n(SO2)=1mol-0.2mol=0.8mol,根据热化学方程式:2SO2(g)+O2(g)?2SO3(g)△H=-196.6KJ?mol-1;可知,△H2=0.4△H=0.4×(=-196.6KJ?mol-1)=-78.64KJ?mol-1.
故答案为:-78.64.
故答案为:S(s)+O2(g)═SO2(g)△H=-297 KJ?mol-1;
(2)由由图1可知,参加反应的n(SO2)=1mol-0.2mol=0.8mol,根据热化学方程式:2SO2(g)+O2(g)?2SO3(g)△H=-196.6KJ?mol-1;可知,△H2=0.4△H=0.4×(=-196.6KJ?mol-1)=-78.64KJ?mol-1.
故答案为:-78.64.
点评:本题既考查了燃烧热的概念、热化学方程式书写,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列过程或现象与盐类水解无关的是( )
| A、纯碱溶液去油污 |
| B、铁在潮湿的环境下生锈 |
| C、向氯化铁溶液中滴入氢氧化钠溶液产生红褐色沉淀 |
| D、浓硫化钠溶液有臭味 |
下列说法正确的是( )
| A、在一定条件下,乙烯能与H2发生加成反应,苯不能与H2发生加成反应 |
| B、C2H6O和C4H10都有2种同分异构体 |
| C、乙酸乙酯、乙酸均能与NaOH反应,二者分子中官能团相同 |
| D、淀粉和蛋白质均可水解生成葡萄糖 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、0.1mol?L-1FeCl2溶液:H+、Na+、Cl-、NO3- |
| B、c(OH-)=0.1mol?L-1的溶液:K+、Na+、ClO-、NO3- |
| C、c(H+)=0.1mol?L-1的溶液:K+、Na+、HCO3-、SO42- |
| D、与铝反应产生大量氢气的溶液:Ba2+、Na+、CO32-、NO3- |
下列说法正确的是( )
| A、除稀有气体外的非金属元素都能生成不同价态的含氧酸 |
| B、若ⅡA某元素的原子序数为m,则同周期ⅢA元素的原子序数一定为m+11 |
| C、在BrCH=CHBr分子中,C-Br键采用的成键轨道是sp-p |
| D、由IA族和VIA族元素形成的原子个数比为1:1、电子总数为38的化合物,可能是含有共价键的离子化合物 |
下列四种模型仅由C、H、O三种原子组成,下列说法正确的是( )
| 序号 | 1 | 2 | 3 | 4 |
| 模型示意图 |  |  |  | 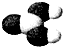 |
| A、模型1对应的物质含有双键 |
| B、1mol模型2对应的物质与足量的银氨溶液充分反应,能生成216gAg |
| C、模型3对应的物质在一定条件下能发生银镜反应 |
| D、模型3、模型4对应的物质均具有酸性,且酸性4强于3 |
 新型纳米材料氧缺位铁酸盐(MFe2OX)(3<x<4;M表示Mn、Co、Zn或Ni的二价离子),常温下,它使能工业废气中的SO2、NO2等氧化物转化为单质.转化流程如图所示:
新型纳米材料氧缺位铁酸盐(MFe2OX)(3<x<4;M表示Mn、Co、Zn或Ni的二价离子),常温下,它使能工业废气中的SO2、NO2等氧化物转化为单质.转化流程如图所示: