题目内容
14.下列物质:①水泥 ②玻璃 ③陶瓷 ④水晶,其中属于硅酸盐工业产品的是( )| A. | 只有①② | B. | 只有②④ | C. | 全部 | D. | 只有①②③ |
分析 硅酸盐工业产品是以含硅物质为原料经加热制成的,包括水泥、陶瓷、玻璃等,以此解答该题.
解答 解:硅酸盐工业产品是以含硅物质为原料经加热制成的,水泥、陶瓷、玻璃的成分中都含有硅酸盐属于硅酸盐工业产品,水晶的成分为二氧化硅,属于氧化物,不属于硅酸盐工业产品,
故选:D.
点评 本题考查硅酸盐产品,侧重于化学与工业生产得到考查,有利于培养学生良好的科学素养,提高学习的积极性,难度较小,明确物质的组成是解答本题的关键,注意基础知识的积累掌握.

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
2.关于下列各装置图的叙述中,不正确的是( )
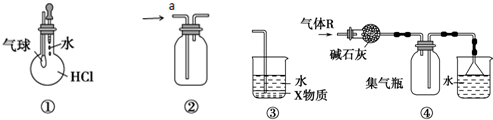

| A. | 装置①可验证HCl气体在水中的溶解性 | |
| B. | 装置②a口进气可用于收集CO2、Cl2或NO等 | |
| C. | 装置③中X为四氯化碳,可用于吸收氨气或氯化氢 | |
| D. | 装置④可用于干燥、收集氨气,并吸收多余的氨气 |
9.在溶液中有Fe3+存在时,则可与它同时大量存在的微粒是( )
| A. | OH- | B. | Fe | C. | H+ | D. | SCN- |
3.根据表中信息,判断以下叙述正确的是部分短周期元素的原子半径及主要化合价( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的稳定性为H2T<H2R | |
| B. | 单质与稀盐酸反应的剧烈程度为L<Q | |
| C. | R最高价氧化物对应水化物是强酸 | |
| D. | L2+与R2-的核外电子数相等 |
4.下列说法中错误的是( )
| A. | 化学视角是现代人所必须具备的科学素养中的重要组成部分 | |
| B. | 元素周期律的发现过程体现了物质分类思想和方法的运用 | |
| C. | 能源是现代文明的原动力,能源的开发和利用离不开化学 | |
| D. | 自然界一切物质都是由离子构成的 |

 +H2O
+H2O .
. 或
或 (任写一种).
(任写一种). 流程的部分信息.
流程的部分信息.