题目内容
10.下列措施中,不能增大化学反应速率的是( )| A. | Zn与稀硫酸反应制取H2时,加入少量硫酸铜 | |
| B. | Al和稀硫酸反应制取H2时,将稀硫酸换成浓硫酸 | |
| C. | 石灰石与稀盐酸反应生成CO2时,将石灰石粉碎 | |
| D. | 用KClO3固体分解制取O2时,固体中添加少量MnO2 |
分析 增大反应物浓度、增大压强、使用催化剂、升高温度、增大接触面积,构成原电池等,均可加快反应速率,而改变纯固体、纯液体的量,反应速率无影响,以此来解答.
解答 解:A、加入少量硫酸铜溶液,铁将铜置换出来与铁形成原电池加快反应速率,故A错误;
B.Al与浓硫酸发生钝化,不生成氢气,反应速率减小,故B正确;
C.块状大理石改为粉末状,增大了接触面积,反应速率加快,故C错误;
D.使催化剂加快化学反应速率,故D错误;
故选B.
点评 本题考查化学反应速率的影响因素,为高频考点,把握常见的影响因素为解答的关键,注重基础知识的考查,选项B为解答的易错点,题目难度不大.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
1.下列溶液可以盛放在玻璃试剂瓶中但不能用磨口玻璃塞的是( )
| A. | 稀盐酸溶液 | B. | 氢氟酸 | C. | 氢氧化钠溶液 | D. | 氯化钠溶液 |
18.下列物质属于纯净物的是( )
| A. | 普通玻璃 | B. | 空气 | C. | 漂白粉 | D. | 干冰 |
5.1mol硫酸铁与1mol铁恰好完全反应,则产物的物质的量为( )
| A. | 1mol | B. | 2mol | C. | 3mol | D. | 4mol |
15.常温下,某溶液中H+的物质的量浓度是OH-的10000倍,该溶液的PH值是( )
| A. | 5 | B. | 8 | C. | 9 | D. | 6 |
19.下列关于 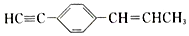 的说法中不正确的是( )
的说法中不正确的是( )
 的说法中不正确的是( )
的说法中不正确的是( )| A. | 最多只有5个碳原子在同一直线上 | B. | 最多有11个碳原子在同一平面上 | ||
| C. | 有7个碳原子可能在同一直线上 | D. | 最多有19个原子在同一平面上 |
20.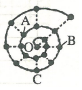 小明在研究元素时发现,可以将前18号元素排成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )
小明在研究元素时发现,可以将前18号元素排成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )
 小明在研究元素时发现,可以将前18号元素排成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )
小明在研究元素时发现,可以将前18号元素排成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点代表氢元素.下列说法中错误的是( )| A. | 虚线相连的元素处于同一族,A元素位于元素周期表ⅥA族 | |
| B. | 离O点越远的元素原子半径一定越大 | |
| C. | B、C最高价氧化物的水化物可以相互反应 | |
| D. | B元素是图中金属性最强的元素 |