题目内容
14.能正确表示下列反应的离子方程式是( )| A. | Na2S水解:S2-+2 H2O?H2S+2OH- | |
| B. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ | |
| C. | 向次氯酸钙溶液通入过量CO2:Ca2++2CIO-+H2O+CO2═CaCO3↓+2HClO | |
| D. | 向次氯酸钙溶液通入SO2:Ca2++2CIO-+H2O+SO2═CaSO3↓+2HClO |
分析 A.硫离子的水解分步进行,离子方程式主要以第一步为主;
B.氢氧化铁更难溶,实现了沉淀的转化;
C.二氧化碳过量,反应生成碳酸氢钙和次氯酸;
D.次氯酸具有强氧化性,能够将亚硫酸钙氧化成硫酸钙.
解答 解:A.Na2S水解分步进行,其主要以第一步水解为主,正确的离子方程式为:S2-+H2O?HS-+OH-,故A错误;
B.向FeCl3溶液中加入Mg(OH)2,反应的离子方程式为:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+,故B正确;
C.向次氯酸钙溶液通入过量CO2,反应生成的是碳酸氢钙,正确的离子方程式为:ClO-+H2O+CO2═HCO3-+HClO,故C错误;
D.向次氯酸钙溶液通入SO2,二者发生氧化还原反应,当二氧化硫足量时,反应的离子反应为:Ca2++2ClO-+2SO2+2H2O=CaSO4↓+SO42-+4H++2Cl-,故D错误;
故选B.
点评 本题考查了离子方程式的正误判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
7.下列各组微粒半径之比大于1的是( )
| A. | $\frac{{{r}_{N{a}^{+}}}^{\;}}{{r}_{Na}}$ | B. | $\frac{{r}_{Mg}}{{r}_{Na}}$ | C. | $\frac{{r}_{p}}{{r}_{Cl}}$ | D. | $\frac{{r}_{N}}{{r}_{p}}$ |
19.无论在酸性溶液还是在碱性溶液中,都能大量共存的离子组是( )
| A. | Na+、Ba2+、S2-、SO42- | B. | Na+、Cu2+、SO42-、Cl- | ||
| C. | Br-、Ba2+、Cl-、K+ | D. | Ca2+、K+、CO32-、NO3- |
6.“嫦娥二号”探月卫星于2010年10月1日18时59分57秒在西昌卫星发射中心发射升空,并获得了圆满成功.据悉,发射“嫦娥二号”探月卫星发射任务的长征三号丙运载火箭使用肼为燃料.已知肼的化学式为N2H4,若1g肼中含有的原子总数为a,则阿伏加德罗常数NA的数值可表示为( )
| A. | $\frac{16a}{3}$ | B. | a | C. | 32a | D. | $\frac{a}{32}$ |
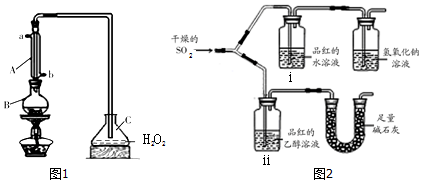
 某课外小组欲鉴定某硫酸钠样品中是否含有亚硫酸钠,设计方案如下:取少量固体配成溶液,往溶液中滴加少量酸性KMnO4溶液,观察溶液是否褪色.如果溶液紫色褪去,说明该样品中含有亚硫酸钠.
某课外小组欲鉴定某硫酸钠样品中是否含有亚硫酸钠,设计方案如下:取少量固体配成溶液,往溶液中滴加少量酸性KMnO4溶液,观察溶液是否褪色.如果溶液紫色褪去,说明该样品中含有亚硫酸钠.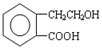 ,它可通过不同化学反应分别制得B、C和D 三种物质.
,它可通过不同化学反应分别制得B、C和D 三种物质.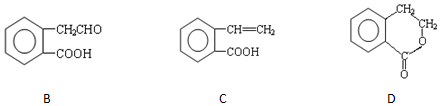
 +H2O
+H2O
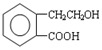 .
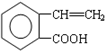
.

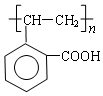 .
.