题目内容
12.a、b、c、d为短周期元素,a的M电子层有1个电子,b的一种核素14b常用于鉴定文物年代,c的最高价化合物与最低价化合物代数和为4,d的低价含氧酸能杀菌、消毒、漂白.下列叙述不正确的是( )| A. | 最高价含氧酸酸性:d>c>b | |
| B. | 它们均存在两种或两种以上的氧化物 | |
| C. | b与氢形成的化合物只存在极性共价键 | |
| D. | a、b、c的离子半径依次增大 |
分析 a、b、c、d为短周期元素,a的M电子层有1个电子,a为Na元素;b的一种核素14b常用于鉴定文物年代,b为C元素;c的最高价化合物与最低价化合物代数和为4,c为S元素;d的低价含氧酸能杀菌、消毒、漂白,d为Cl元素,以此来解答.
解答 解:由上述分析可知,a为Na,b为C,c为S,d为Cl,
A.非金属性d>c>b,则最高价含氧酸酸性:d>c>b,故A正确;
B.存在氧化钠、过氧化钠、CO、二氧化碳、二氧化硫、三氧化硫、ClO2、Cl2O7等,故B正确;
C.乙烷中含C-C非极性键,故C错误;
D.电子层越多,离子半径越大,具有相同电子排布时原子序数大的离子半径小,则a、b、c的离子半径依次增大,故D正确;
故选C.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、元素的性质、元素化合物知识推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.向14.8g Fe2O3、FeO和Cu的混合物中,加入1mol•L-1硫酸溶液200mL时,固体恰好完全溶解,所得溶液中不含Fe3+.若用足量的CO在高温下还原相同质量的原混合物,得到的固体质量为( )
| A. | 11.6g | B. | 10.8g | C. | 8.4g | D. | 13.2g |
6.下列实验能达到相关实验目的是( )
| A. | 用新制的Cu(OH)2悬浊液检验淀粉是否水解完全 | |
| B. | 先滴加KSCN溶液无明显现象,再滴加H2O2溶液,检验溶液中是否含Fe2+ | |
| C. | 加热氯化铵固体制取适量氨气 | |
| D. | 用饱和碳酸氢钠溶液除去Cl2中含有的HCl |
1.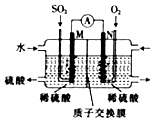 某兴趣小组用电化学法模拟工业处理SO2.强硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验.下列说法正确的是( )
某兴趣小组用电化学法模拟工业处理SO2.强硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验.下列说法正确的是( )
 某兴趣小组用电化学法模拟工业处理SO2.强硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验.下列说法正确的是( )
某兴趣小组用电化学法模拟工业处理SO2.强硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验.下列说法正确的是( )| A. | N极为负极 | |
| B. | 反应一段时间后,左侧电解质溶液的pH增大 | |
| C. | M极发生的电极反应为SO2+2H2O-2e-═SO42-+4H+ | |
| D. | 在相同条件下,M、N两极上消耗的气体体积之比为1:2 |
7.下列有关实验原理或实验操作正确的是( )
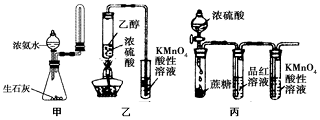

| A. | 实验室用图甲所示装置制取少量氨气 | |
| B. | 为使100ml0.5mol/L的NaNO3溶液物质的量浓度变为1mol/L,可将原溶液加热蒸发掉50ml水 | |
| C. | 利用图乙装置,可制取乙烯并验证其易被酸性KMnO4溶液氧化 | |
| D. | 利用图丙装置,可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |
4.下列说法不正确的是( )
| A. | 等物质的量的乙烯和乙醇完全燃烧消耗氧气的量相等 | |
| B. | 戊烷和2-甲基丁烷是同系物 | |
| C. | 甲烷的二氯代物只有一种的事实,可证明甲烷为正四面体结构 | |
| D. | 三硝酸甘油酯的分子式为C3H5N3O9 |
1.化学在日常生活中应用广泛,下列叙述及对应关系错误的是( )
| 实际应用 | 相应性质 | |
| A | 用含有酸性重铬酸钾溶液的仪器检验酒后驾车 | 乙醇具有还原性 |
| B | 明矾常用于自来水的净化、杀菌消毒 | 明矾可发生水解生成胶状的Al(OH)3 |
| C | BaSO4可作为造影剂检查肠胃道疾病 | BaSO4难溶于水且不与盐酸反应 |
| D | 过氧化钠可用作呼吸面具中的供氧剂 | Na2O2能与CO2反应生成O2 |
| A. | A | B. | B | C. | C | D. | D |
3.某非金属单质气体Y2在加热条件下,1mol Y2 (g)与80克烧碱恰好完全反应,生成NaY、H2O和另一种气体,该气体是下列中的( )
| A. | H2 | B. | HY | C. | Y2 O | D. | O2 |



