题目内容
3.某非金属单质气体Y2在加热条件下,1mol Y2 (g)与80克烧碱恰好完全反应,生成NaY、H2O和另一种气体,该气体是下列中的( )| A. | H2 | B. | HY | C. | Y2 O | D. | O2 |
分析 n(NaOH)=$\frac{80g}{40g/mol}$=2mol,则n(NaOH):n(Y2)=2:1,发生Y2+2NaOH═2NaY+H2O+X↑,以此来解答.
解答 解:n(NaOH)=$\frac{80g}{40g/mol}$=2mol,则n(NaOH):n(Y2)=2:1,发生Y2+2NaOH═2NaY+H2O+X↑,Y元素的化合价降低,结合电子守恒及原子守恒可知,X含O元素,且化合价升高,反应为2Y2+4NaOH═4NaY+2H2O+O2↑,即另一种气体为O2,
故选D.
点评 本题考查氧化还原反应,为高频考点,把握习题中的信息及守恒法为解答的关键,侧重分析与应用能力的考查,注意O元素化合价升高的判断,题目难度不大.

练习册系列答案
相关题目
12.a、b、c、d为短周期元素,a的M电子层有1个电子,b的一种核素14b常用于鉴定文物年代,c的最高价化合物与最低价化合物代数和为4,d的低价含氧酸能杀菌、消毒、漂白.下列叙述不正确的是( )
| A. | 最高价含氧酸酸性:d>c>b | |
| B. | 它们均存在两种或两种以上的氧化物 | |
| C. | b与氢形成的化合物只存在极性共价键 | |
| D. | a、b、c的离子半径依次增大 |
13.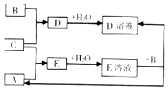 短周期元素X、Y、Z的原子序数依次增大,其中Y元素的原子半径最大.已知A、B、C分别是X、Y、Z三种元素的单质,A和C常温下为气体.在适宜的条件下,A、B、C可以发生如图所示的反应.下列说法正确的是( )
短周期元素X、Y、Z的原子序数依次增大,其中Y元素的原子半径最大.已知A、B、C分别是X、Y、Z三种元素的单质,A和C常温下为气体.在适宜的条件下,A、B、C可以发生如图所示的反应.下列说法正确的是( )
 短周期元素X、Y、Z的原子序数依次增大,其中Y元素的原子半径最大.已知A、B、C分别是X、Y、Z三种元素的单质,A和C常温下为气体.在适宜的条件下,A、B、C可以发生如图所示的反应.下列说法正确的是( )
短周期元素X、Y、Z的原子序数依次增大,其中Y元素的原子半径最大.已知A、B、C分别是X、Y、Z三种元素的单质,A和C常温下为气体.在适宜的条件下,A、B、C可以发生如图所示的反应.下列说法正确的是( )| A. | 化合物YX中含离子键 | B. | Z的含氧酸均为强酸 | ||
| C. | 非金属性:X>Z | D. | 离子半径:Y>Z |
10.用NA表示阿佛加德罗常数的值,下列说法正确的是( )
| A. | 在浓硫酸作用下,60g冰醋酸与足量无水乙醇反应生成乙酸乙酯的分子数为NA | |
| B. | 标准状况下,3.36LC2H4和C3H6的混合气体中含有碳碳双键的数目为0.15NA | |
| C. | 电解精炼铜,当外电路转移NA个电子时,阳极质量减少32g | |
| D. | 含0.01molFeCl3的浓溶液滴入沸水,制得的胶体粒子数目小于0.01NA |
17.已知1~20号元素的离子,aW2+、bX+、cY2-、dZ-都具有相同的电子层结构,下列说法正确的是( )
| A. | 质子数:d>c>b>a | B. | 离子半径:W2+>X+>Y2->Z- | ||
| C. | 原子半径:Z<Y<W<X | D. | 最低负价:X<W<Z<Y |