题目内容
14.同主族3种元素X、Y、Z,已知它们的最高价氧化物对应水化物的酸性HXO4>HYO4>HZO4,则下列判断正确的是( )| A. | 原子半径X>Y>Z | B. | 气态氢化物稳定性 HX<HY<HZ | ||
| C. | 非金属性X>Y>Z | D. | 阴离子的还原性X->Y->Z- |
分析 同主族元素从上到下元素的非金属性逐渐减弱,元素的非金属性越强,对应的最高价氧化物对应水化物的酸性越强,已知最高价氧化物对应水化物的酸性:HXO4>HYO4>HZO4,则非金属性X>Y>Z,以此判断元素对应单质、化合物的性质.
解答 解:同主族元素对应最高价氧化物对应水化物的酸性:HXO4>HYO4>HZO4,则非金属性X>Y>Z,则
A.同主族元素从上到下元素的非金属性逐渐减弱,原子半径逐渐增大,则原子半径:X<Y<Z,故A错误;
B.非金属性越强,则其气态氢化物的稳定性越强,非金属性X>Y>Z,则气态氢化物稳定性 HX>HY>HZ,故B错误;
C.同主族元素对应最高价氧化物对应水化物的酸性:HXO4>HYO4>HZO4,则非金属性X>Y>Z,故C正确;
D.非金属性越强,则其阴离子的还原性越弱,非金属性X>Y>Z,则阴离子的还原性X-<Y-<Z-,故D错误.
故选C.
点评 本题考查同主族元素的性质的递变规律,为高考常见题型,题目难度不大,本题注意把握元素周期律的递变规律以及元素对应的单质、化合物的性质.

练习册系列答案
相关题目
5.已知aA+、bB2+、cC-、dD2-四种离子均具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是( )
| A. | 原子半径:A>B>C>D | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:D>C>B>A | D. | a+1=d-2 |
9.向铁和氧化铁的混合物中加入足量的稀H2SO4,充分反应后生成FeSO4溶液,当生成的Fe2+和H2的物质的量之比为4:1时,被氧化的铁与被还原的铁的物质的量之比是( )
| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 1:3 |
19.氮的氢化物NH3和N2H4有广泛应用.
(1)已知25℃时,几种难溶电解质的溶度积如下表所示:
向Cu2+、Mg2+、Fe3+、Fe2+浓度都为0.01mol•L-1的溶液中缓慢滴加稀氨水,产生沉淀的先后顺序为 (用化学式表示)Fe(OH)3、Cu(OH)2、Fe(OH)2、Mg(OH)2.
(2)实验室制备氨气的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.工业上,制备肼(N2H4)的方法之一是用次氯酸钠溶液在碱性条件下与氨气反应.以石墨为电极,将该反应设计成原电池,该电池的负极反应为2NH3+2OH--2e-═N2H4+2H2O.
(3)在3L密闭容器中,起始投入4molN2和9molH2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
已知:破坏1molN2(g)和3molH2(g)中的化学键消耗的总能量小于破坏2molNH3(g)中的化学键消耗的能量.
①则T1<T2(填“>”、“<”或“=”)
②在T2K下,经过10min达到化学平衡状态,则0~10min内H2的平均速率v(H2)=0.1 mol•L-1•min-1,平衡时N2的转化率α(N2)=25%.若再增加氢气浓度,该反应的平衡常数将不变(填“增大”、“减小”或“不变”)
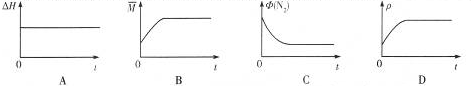
③下列图象分别代表焓变(△H)、混合气体平均相对分子质量( $\overline{M}$)、N2体积分数φ(N2)和气体密度(ρ)与反应时间关系,其中正确且能表明该可逆反应达到平衡状态的是BC.
(1)已知25℃时,几种难溶电解质的溶度积如下表所示:
| 氢氧化物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
| Ksp | 2.2×10-20 | 4.0×10-38 | 8.0×10-16 | 1.8×10-11 |
(2)实验室制备氨气的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.工业上,制备肼(N2H4)的方法之一是用次氯酸钠溶液在碱性条件下与氨气反应.以石墨为电极,将该反应设计成原电池,该电池的负极反应为2NH3+2OH--2e-═N2H4+2H2O.
(3)在3L密闭容器中,起始投入4molN2和9molH2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
| 温度(K) | 平衡时NH3的物质的量(mol) |
| T1 | 2.4 |
| T2 | 2.0 |
①则T1<T2(填“>”、“<”或“=”)
②在T2K下,经过10min达到化学平衡状态,则0~10min内H2的平均速率v(H2)=0.1 mol•L-1•min-1,平衡时N2的转化率α(N2)=25%.若再增加氢气浓度,该反应的平衡常数将不变(填“增大”、“减小”或“不变”)
③下列图象分别代表焓变(△H)、混合气体平均相对分子质量( $\overline{M}$)、N2体积分数φ(N2)和气体密度(ρ)与反应时间关系,其中正确且能表明该可逆反应达到平衡状态的是BC.

4.下列溶液中的Cl-浓度与1mol/LMgCl2溶液中的Cl-浓度相等的是( )
| A. | 1mol/L NaCl溶液 | B. | 1 mol/LCaCl2溶液 | ||
| C. | 1 mol/L KCl溶液 | D. | 1 mol/LAlCl3溶液 |
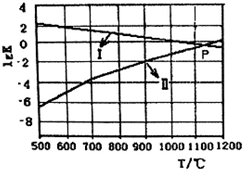 一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,可以减少SO2的排放,但产生的CO又会与CaSO4发生化学反应,从而降低脱硫效率.相关的热化学方程式如下:
一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,可以减少SO2的排放,但产生的CO又会与CaSO4发生化学反应,从而降低脱硫效率.相关的热化学方程式如下: ,离子键,共价键;
,离子键,共价键;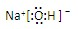 ,离子键,共价键;
,离子键,共价键; ;共价键;
;共价键; ,共价键,离子键.
,共价键,离子键.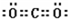 ;共价键;
;共价键; ;共价键.
;共价键.