题目内容
3.下列表示对应化学反应的离子方程式正确的是( )| A. | 等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| B. | 用两个铜电极电解CuSO4 溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$ 2Cu↓+O2↑+4H+ | |
| C. | 硫酸氢钠溶液与氢氧化钡溶液恰好反应呈中性:H++SO42-+Ba2++OH-═H2O+BaSO4↓ | |
| D. | 向含有0.1 mol溶质的硫酸亚铁稀溶液中加入7.8 g Na2O2:4Na2O2+4Fe2++6H2O═4Fe(OH)3+8Na++O2↑ |
分析 A.该离子方程式缺少酸和碱的中和反应;
B.用两个铜电极电解CuSO4 溶液,阳极为铜本身失电子变成铜离子,阴极溶液中的铜离子在阴极析出,没有水参与电解;
C.反应后的溶液为中性,则氢离子与氢氧根离子的物质的量相等;
D.过氧化钠和水反应生成氢氧化钠和氧气,氧气氧化亚铁离子为三价铁离子,和氢氧化钠生成氢氧化铁沉淀.
解答 解:A.等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++4OH-+2H+═Mg(OH)2↓+2H2O,故A错误;
B.用铜电极电解CuSO4溶液时,阳极为铜本身失电子变成铜离子,阴极溶液中的铜离子在阴极析出,这时相当于电镀装置,没有水参与电解,故B错误;
C.硫酸氢钠溶液与氢氧化钡溶液恰好反应呈中性,硫酸氢钠与氢氧化钡按照物质的量2:1反应,反应的离子方程式为:2H++SO42-+Ba2++2OH-=2H2O+BaSO4↓,故C错误;
D.过氧化钠和水反应生成氢氧化钠和氧气,氧气氧化亚铁离子为三价铁离子,和氢氧化钠生成氢氧化铁沉淀;向含有0.1 mol溶质的硫酸亚铁稀溶液中加入7.8 g Na2O2,Na2O2的物质的量为0.1mol,亚铁离子和过氧化钠等物质的量反应,离子方程式为:4Na2O2+4Fe2++6H2O=4Fe(OH)3+8Na++O2↑,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,题目难度中等,把握发生的化学反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关的离子反应、电解反应的考查.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
14.下列有关实验说法正确的是( )
| A. | 金属钠长期露置在空气中,最终生成碳酸钠,中间有Na2O2生成 | |
| B. | 比较去锈的铁钉和去锈的绕有细铜丝的铁钉与同浓度盐酸反应速率快慢时,可以加几滴KSCN溶液,观察铁钉周围出现出现血红色现象的快慢 | |
| C. | 原电池的制作:用导线把二极管和锌片、铜片连接起来,锌与铜之间隔一块薄海绵放入稀H2SO4 溶液,二极管发光但很快变暗,若再加入H2O2瞬间又变亮且能持续较长时间 | |
| D. | 在蔗糖中滴加浓硫酸产生的气体,能使酸性KMnO4溶液褪色,说明该气体具有漂白性 |
15.实验室模拟“人工树叶”将H2O和CO2转化为O2和C6Hl2O6,以下说法正确的是( )
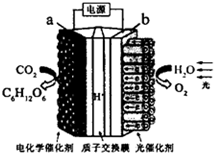

| A. | a极与电源的正极相连 | |
| B. | 该装置能量转化形式仅为电能转化为化学能 | |
| C. | 阳极反应为 6COz+24H+-24e-=C6Hl206+6H20 | |
| D. | 电解后阳极区溶液的pH不变(忽略体积影响) |
12.下列有关实验操作、现象或结论的叙述正确的是( )
| A. | 石油的蒸馏实验中,加入碎瓷片可防止石油在蒸馏时暴沸 | |
| B. | 乙醇的催化氧化实验中铜丝主要起氧化剂的作用 | |
| C. | 制取乙酸乙酯时,试剂加入的顺序是:先加入乙醇,后慢慢加入乙酸,最后加入浓硫酸 | |
| D. | 在淀粉溶液中加入少量稀硫酸,水浴加热后,再加入少量新制的氢氧化铜悬浊液,加热至沸腾,没有砖红色沉淀生成,说明淀粉没有水解 | |
| E. | 除去甲烷中混有的少量乙烯,可以将混合气体通过酸性溶KMnO4液 | |
| F. | 用钠可以检验某无水酒精中是否含有水 | |
| G. | 可用溴水来鉴别植物油和矿物油 |
 )是临床一种应用广泛的药物,它的一条合成路线如下:
)是临床一种应用广泛的药物,它的一条合成路线如下:

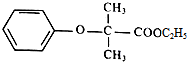 .
. 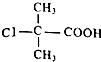 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$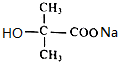 +NaCl+H2O.
+NaCl+H2O.  印尼火山喷发不仅带来壮观的美景,还给附近的居民带来物质财富,有许多居民冒着生命危险在底部的火山口收集纯硫磺块来赚取丰厚收入.硫磺可用于生产化工原料硫酸.某工厂用如图所示的工艺流程生产硫酸:
印尼火山喷发不仅带来壮观的美景,还给附近的居民带来物质财富,有许多居民冒着生命危险在底部的火山口收集纯硫磺块来赚取丰厚收入.硫磺可用于生产化工原料硫酸.某工厂用如图所示的工艺流程生产硫酸:

 ;FHCOOCH=CH2;
;FHCOOCH=CH2;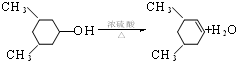 ;反应④HCOOCH=CH2+H2O$→_{△}^{浓硫酸}$HCOOH+CH3CHO.
;反应④HCOOCH=CH2+H2O$→_{△}^{浓硫酸}$HCOOH+CH3CHO.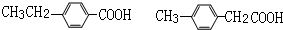 .
.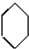 $→_{①}^{Cl_{2},光照}$
$→_{①}^{Cl_{2},光照}$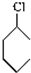 $→_{△②}^{NaOH醇溶液}$A$→_{③}^{Cl_{2},不见光}$B$\stackrel{④}{→}$
$→_{△②}^{NaOH醇溶液}$A$→_{③}^{Cl_{2},不见光}$B$\stackrel{④}{→}$ $\stackrel{⑤}{→}$
$\stackrel{⑤}{→}$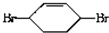 $\stackrel{⑥}{→}$$→_{H_{2}}^{⑦}$
$\stackrel{⑥}{→}$$→_{H_{2}}^{⑦}$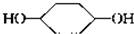
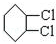 ,C
,C
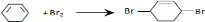 .
.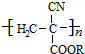 从而具有胶黏性.某种氰基丙烯酸酯(G)的合成路线如下:
从而具有胶黏性.某种氰基丙烯酸酯(G)的合成路线如下: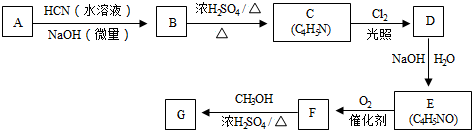
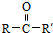 $→_{NaOH(微量)}^{HCN(水溶液)}$
$→_{NaOH(微量)}^{HCN(水溶液)}$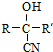
 .其核磁共振氢谱显示为2组峰,峰面积比为1:6.
.其核磁共振氢谱显示为2组峰,峰面积比为1:6. +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$ +NaCl.
+NaCl.