题目内容
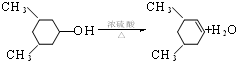
18.已知:通常羟基与烯键碳原子相连接时,易发生下列转化:
现有下列所示的转化关系:

已知:B、G、F均能发生银镜反应,C能与浓溴水发生反应产生分子式为C8H7Br3O白色沉淀,C的核磁共振氢谱中只出现4组峰.E能使溴水褪色.
请回答:
(1)结构简式:C
 ;FHCOOCH=CH2;
;FHCOOCH=CH2;(2)写出③的反应类型消去反应;
(3)完成下列反应的化学方程式:反应③
 ;反应④HCOOCH=CH2+H2O$→_{△}^{浓硫酸}$HCOOH+CH3CHO.
;反应④HCOOCH=CH2+H2O$→_{△}^{浓硫酸}$HCOOH+CH3CHO.(4)写出符合下列条件的“A”的所有同分异构体:
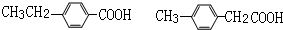 .
.①能与碳酸氢钠溶液发生反应;②核磁共振氢谱中出现五组峰③含有一个苯环.
分析 F能发生加聚反应,说明含有碳碳双键,可发生水解,应含有酯基,且水解产物B、G均能发生银镜反应,说明水解生成HCOOH,由于羟基连接碳碳双键不稳定,转化为-CHO,则另一种物质为CH3CHO,A能在酸性条件下水解,应为酯,水解产物B为HCOOH,则G为CH3CHO,C能与浓溴水发生反应产生白色沉淀,说明C含有酚羟基,C的核磁共振氢谱中只出现4组峰,结构应对称,则A为 ,故C为
,故C为 ,D为
,D为 ,E含有碳碳双键,能使溴水褪色,则E为
,E含有碳碳双键,能使溴水褪色,则E为 .
.
解答 解:F能发生加聚反应,说明含有碳碳双键,可发生水解,应含有酯基,且水解产物B、G均能发生银镜反应,说明水解生成HCOOH,由于羟基连接碳碳双键不稳定,转化为-CHO,则另一种物质为CH3CHO,A能在酸性条件下水解,应为酯,水解产物B为HCOOH,则G为CH3CHO,C能与浓溴水发生反应产生白色沉淀,说明C含有酚羟基,C的核磁共振氢谱中只出现4组峰,结构应对称,则A为 ,故C为
,故C为 ,D为
,D为 ,E含有碳碳双键,能使溴水褪色,则E为
,E含有碳碳双键,能使溴水褪色,则E为 .
.
(1)由以上分析可知,C为 ,F为HCOOCH=CH2,
,F为HCOOCH=CH2,
故答案为: ;HCOOCH=CH2;
;HCOOCH=CH2;
(2)反应③是 发生消去反应生成
发生消去反应生成 ,
,
故答案为:消去反应;
(3)反应③的化学反应方程式为: ,
,
反应④的化学反应方程式:HCOOCH=CH2+H2O$→_{△}^{浓硫酸}$HCOOH+CH3CHO,
故答案为: ;HCOOCH=CH2+H2O$→_{△}^{浓硫酸}$HCOOH+CH3CHO;
;HCOOCH=CH2+H2O$→_{△}^{浓硫酸}$HCOOH+CH3CHO;
(4)A( )的同分异构体,符合下列条件:①能与碳酸氢钠溶液发生反应,说明含有-COOH,②核磁共振氢谱中出现五组峰,③含有一个苯环,符合条件的同分异构体有:
)的同分异构体,符合下列条件:①能与碳酸氢钠溶液发生反应,说明含有-COOH,②核磁共振氢谱中出现五组峰,③含有一个苯环,符合条件的同分异构体有: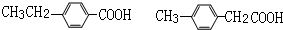 ,
,
故答案为: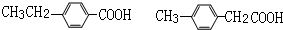 .
.
点评 本题考查有机物的推断,注意根据F和C性质进行推断,熟练掌握官能团的性质与转化,综合考查学生分析能力和综合运用化学知识的能力,题目难度中等.

| A. | 中国古代的陶瓷是以黏土为原料,经高温烧结而成的 | |
| B. | 古代染坊常用某种“碱剂”来精炼丝绸,该“碱剂”的主要成分是火碱 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化 | |
| D. | 家庭使用“84”消毒液时,为增强消毒效果,可以加入洁厕灵(含有强酸) |
| A. | 取少量含稀硫酸的淀粉水解液于试管中,加入过量的NaOH溶液,再滴加少量碘水以检验淀粉是否完全水解 | |
| B. | 向AlCl3溶液中逐滴滴加NaOH溶液至过量,可证明Al(OH)3是两性氢氧化物 | |
| C. | 酸碱中和滴定时,用强酸滴定强碱通常滴加2~3滴甲基橙做指示剂,若甲基橙加入过多对实验无影响 | |
| D. | 在砂纸打磨过的铁片上滴几滴含酚酞的饱和食盐水,静置1~2 min,会观察到在液滴的边缘位置先出现红色 |
| A. | S在过量氧气中燃烧生成SO3 | |
| B. | 浓硫酸具有吸水性,但不可干燥氨气和二氧化硫 | |
| C. | NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中 | |
| D. | 锌与足量稀硫酸反应,滴入几滴硫酸铜溶液,可使反应速率加快,又不影响生成气体的量 |
| 选项 | 操作 | 现象 | 结论 |
| A. | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液显紫红色 | 氧化性: Fe3+>I2 |
| B. | 向盛有Na2SiO3溶液的试管中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2min后,试管里出现凝胶 | 非金属性: Cl>Si |
| C. | 2mL 0.1mol/L的NaOH溶液中滴加2滴0.1mol/L的MgCl2溶液,再滴加2滴0.1mol/L的FeCl3溶液(每滴约0.02ml) | 先出现白色沉淀后又有红褐色沉淀产生 | 溶解度: Fe(OH)3>Mg(OH)2 |
| D. | 向H2S溶液中滴加CuSO4溶液 | 有黑色沉淀(成分为CuS)产生 | 酸性: H2S>H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| B. | 用两个铜电极电解CuSO4 溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$ 2Cu↓+O2↑+4H+ | |
| C. | 硫酸氢钠溶液与氢氧化钡溶液恰好反应呈中性:H++SO42-+Ba2++OH-═H2O+BaSO4↓ | |
| D. | 向含有0.1 mol溶质的硫酸亚铁稀溶液中加入7.8 g Na2O2:4Na2O2+4Fe2++6H2O═4Fe(OH)3+8Na++O2↑ |
 化合物M(fumimycin)是从微生物中分离得到的,它显示出广谱抗菌活性.下列关于化合物M的说法中错误的是( )
化合物M(fumimycin)是从微生物中分离得到的,它显示出广谱抗菌活性.下列关于化合物M的说法中错误的是( )| A. | 化合物M能使酸性KMnO4溶液褪色 | |
| B. | 化合物M在强酸中水解可生成 | |
| C. | 化合物M分子间能形成氢键 | |
| D. | 1 mol M在NaOH溶液中反应,最多消耗5 mol NaOH |
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向某溶液中滴加少量NaOH稀溶液,用湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| B | NaHCO3溶液与NaAlO2溶液混合 | 生成白色沉淀 | 结合H+的能力:AlO2-<CO32- |
| C | 向水玻璃溶液中通入足量CO2 | 产生白色浑浊 | 酸性:H2CO3>H2SiO3 |
| D | 向FeCl3溶液中通入足量SO2气体 | 黄色退去 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 乙烯和乙醇 | B. | 苯和氯乙烯 | C. | 乙酸和溴乙烷 | D. | 丙烯和丙烷 |