题目内容
15.下列各组物质中,用溴水或高锰酸钾酸性溶液均能鉴别的是( )| A. | 1-己烯、苯 | B. | 乙烯、乙炔 | C. | 甲苯、苯 | D. | 己烷、戊烷 |
分析 用高锰酸钾酸性溶液和溴水,其中一种物质应含有C=C,可被高锰酸钾氧化,与溴水发生加成反应,以此解答该题.
解答 解:A.苯和溴水、高锰酸钾不反应,但1-己烯能与高锰酸钾发生氧化反应,与溴水发生加成反应,可鉴别,故A正确;
B.乙烯、乙炔都能被高锰酸钾氧化,都与溴水发生加成反应,不能鉴别,故B错误;
C.苯和甲苯与溴水都不反应,不能鉴别,故C错误;
D.己烷、戊烷与高锰酸钾酸性溶液和溴水都不反应,不能鉴别,故D错误.
故选A.
点评 本题考查有机物的鉴别,为高频考点,把握物质的性质、发生的反应与现象为解答的关键,侧重分析与应用能力的考查,注意有机物官能团与性质,题目难度不大.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
5.次磷酸(H3PO2)是一种精细磷化工产品,属于一元弱酸,具有较强的还原性.下列有关说法正确的是( )
| A. | H3PO2溶于水的电离方程式为:H3PO2?H++H2PO2- | |
| B. | H3PO2与过量NaOH溶液反应的离子方程式为:H3PO2+3OH-═PO23-+3H2O | |
| C. | 将H3PO2溶液加入到酸性高锰酸钾溶液中,H3PO2的还原产物为H3PO4 | |
| D. | 用惰性电极电解NaH2PO2溶液,其阳极反应式为:2H2O-4e-═O2↑+4H+ |
3.在核电荷数为1~36的元素中,原子的最外层电子排布满足4S1的元素共有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
20.下列说法中不正确的是( )
| A. | 周期表中金属与非金属的分界线附近可以找到半导体 | |
| B. | 周期表中F是最活泼的非金属,Li是最活泼的金属 | |
| C. | 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共18个纵行 | |
| D. | X2+的核外电子数目为18,则X在第四周期第ⅡA族 |
7.现有几组物质的熔点(℃)数据:
据此回答下列问题:
(1)A组属于原子晶体,其熔化时克服的微粒间的作用力是共价键.
(2)C组中HF熔点反常是由于HF分子间能形成氢键,其熔化时需要消耗的能量更多.
(3)D组晶体可能具有的性质是②④(填序号).
①硬度非常高 ②水溶液能导电 ③固体能导电 ④熔融状态能导电.
| A组 | B组 | C组 | D组 |
| 金刚石:3 550℃ | Li:181℃ | HF:-83℃ | NaCl:801℃ |
| 硅晶体:1 410℃ | Na:98℃ | HCl:-115℃ | KCl:776℃ |
| 硼晶体:2 300℃ | K:64℃ | HBr:-89℃ | RbCl:718℃ |
| 二氧化硅:1 723℃ | Rb:39℃ | HI:-51℃ | CsCl:645℃ |
(1)A组属于原子晶体,其熔化时克服的微粒间的作用力是共价键.
(2)C组中HF熔点反常是由于HF分子间能形成氢键,其熔化时需要消耗的能量更多.
(3)D组晶体可能具有的性质是②④(填序号).
①硬度非常高 ②水溶液能导电 ③固体能导电 ④熔融状态能导电.
5.某化合物的结构(键线式)及球棍模型如图1:
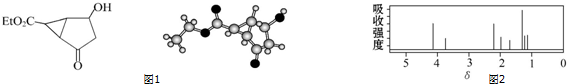
该有机分子的核磁共振氢谱图如图2(单位是ppm):
下列关于该有机物的叙述正确的是( )

该有机分子的核磁共振氢谱图如图2(单位是ppm):
下列关于该有机物的叙述正确的是( )
| A. | 该有机物不同化学环境的氢原子有6种 | |
| B. | 该有机物属于芳香化合物 | |
| C. | 键线式中的Et代表的基团为-CH3 | |
| D. | 该有机物在一定条件下能与金属钠、乙酸发生反应 |
 某研究性学习小组为了探究化学能与热能之间的转化,设计了以下实验装置并按如下操作进行实验:
某研究性学习小组为了探究化学能与热能之间的转化,设计了以下实验装置并按如下操作进行实验: 已知N2和H2在一定条件下发生下列可逆反应:
已知N2和H2在一定条件下发生下列可逆反应: