题目内容
4. 已知N2和H2在一定条件下发生下列可逆反应:
已知N2和H2在一定条件下发生下列可逆反应:N2(g)+3H2?2NH3(g)△H=-92.4kJ.mol-1
(1)若V(正)随时间变化如图,则下列说法一定正确的是B
A.t1时升髙了温度
B.2时使用了催化剂
C.t3时增大了压强
D.t4时降低了温度
(2)若在恒温条件下,将-定量的N2和H2的混合气体通入一个容积为2升固定容积的密闭容器中,5分钟后反应达平衡,且测得平衡时n(N2)=1.2mol.n( H2)=12mol,n(NH3)=0.8mol,则反应速率V(N2)=_0.04mol.L-1•min-1,平衡常数=1.23×10-3(mol/L)-2(计算结果保留小数点后2位)
(3)若在某温度下,将1体积N2和3体积H2通人一个容积为2升固定容积的密闭容器中,5分钟后反应达平衡,且测得平衡时NH3占总体积的12%,则N2占总体积的22%.
分析 (1)升高温度、增大压强正反应速率离开原来的速率点迅速增加,加入催化剂,反应速率加快,但是平衡不移动,降低反应物的浓度,速率在原来基础上降低;
(2)先计算氨气平衡时的物质的量计算氮气反应的物质的量,再计算其反应速率,根据起始量和平衡时的量来计算物质的转化率、平衡常数,并利用浓度增大来分析平衡的移动;
(3)在相同条件下,各组分的体积分数就是物质的量分数,根据三行式进行计算.
解答 解:(1)升高温度、增大压强正反应速率离开原来的速率点迅速增加,加入催化剂,反应速率加快,但是平衡不移动,降低反应物的浓度,速率在原来基础上降低;
A.t1时是增大压强,故错误;
B.t2时反应速率加快,但是平衡不移动,使用了催化剂,故正确;
C.t3时是降低了压强,故错误;
D.t4时降低了反应物的浓度,故错误.
故选B;
(2)5分钟后反应达平衡时,n(N2)=1.2mol,n(H2)=1.2mol,n (NH3)=0.8mol,设参加反应的氮气的物质的量为x,则参加反应的氢气的物质的量为3x,则
N2+3H2?2NH3,
1 3 2
x 3x 0.8mol
$\frac{1}{x}=\frac{2}{0.8}$,x=0.4mol,
反应速率V(N2)=$\frac{\frac{0.4mol}{2L}}{5min}$=0.04mol/(L.mim),氢气的转化率为$\frac{3×0.4mol}{3×0.4mol+1.2mol}$×100%=50%,平衡时的浓度分别为c(N2)=0.6mol/L、c(H2)=6mol/L,c(NH3)=0.4mol/L,则平衡常数K=$\frac{0.{4}^{2}}{0.6×{6}^{3}}$=1.23×10-3(mol/L)-2,上述平衡体系中的混合气体的浓度增大1倍,相当于缩小体积,则压强增大,化学平衡正向移动,即向右移动,
故答案为:0.04;1.23×10-3;
(3)将1体积N2和3体积H2通人一个容积为2升固定容积的密闭容器中,5分钟后反应达平衡,且测得平衡时NH3占总体积的12%,设氮气的变化量是x,三行式如下:
N2(g)+3H2?2NH3(g)
初始体积:1 3 0
变化体积:x 3x 2x
平衡体积:1-x 3-3x 2x
$\frac{2x}{1-x+3-3x+2x}$×100%=12%,解得x≈0.214,所以N2占总体积的$\frac{1-0.214}{4-2×0.214}$×100%≈22%,故答案为:22%.
点评 本题考查影响化学反应速率和平衡移动的因素、以及有关三行式的计算知识,注意知识的迁移应用是关键,难度中等.

| A. | 化学反应中一定有化学键断裂,同时也有化学键形成 | |
| B. | 只有共价键的物质一定是共价化合物 | |
| C. | 含有阴离子的化合物一定含有阳离子 | |
| D. | 非金属元素和非金属元素形成的化合物不一定是离子化合物 |
| A. | 1-己烯、苯 | B. | 乙烯、乙炔 | C. | 甲苯、苯 | D. | 己烷、戊烷 |
| A. | A原子的最外层电子数比B原子的最外层电子数少 | |
| B. | A原子电子层数比B原子电子层数多 | |
| C. | 1mol A从酸中置换 H+生成的H2比 1mol B从酸中置换H+生成的H2多 | |
| D. | A金属可以把B金属从其盐溶液中置换出来 |
| A. | 0.1mol•L-1的醋酸加水稀释,$\frac{c({H}^{+})}{c(O{H}^{-})}$减小 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,KW变大 | |
| C. | 体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量)后者用时少 | |
| D. | 常温下,V1L pH=11的NaOH溶液与V2L pH=3的HA溶液混合,若混合液显中性,则V1≤V2 |
| A. | SO2具有漂白性,因而可以使石蕊试液褪色 | |
| B. | 大气中SO2的主要来源是汽车排出的尾气 | |
| C. | SO2是硫酸的酸酐 | |
| D. | SO2既可以是含硫物质的氧化产物,又可以是含硫物质的还原产物 |
| A. | 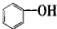 属于醇类化合物 属于醇类化合物 | B. | 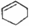 属于芳香族化合物 属于芳香族化合物 | ||
| C. | 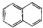 属于脂环化合物 属于脂环化合物 | D. | CH3CH(CH3)2 属于链状化合物 |
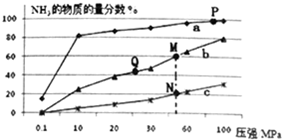 已知N2(g)+3H2(g)?2NH3(g)△H<0,当反应器中按n(N2):n(H2)=1:3投料后,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如图.
已知N2(g)+3H2(g)?2NH3(g)△H<0,当反应器中按n(N2):n(H2)=1:3投料后,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如图.