题目内容
19.在Fe、Cu的混合物中,加入一定量的稀硝酸并微热,充分反应后剩余金属a g.再向其中加入一定量的稀硫酸并加热,充分振荡后剩余金属b g,则( )| A. | a可能等于b | B. | a一定小于b | C. | a可能大于b | D. | a一定大于b |
分析 反应后溶液中存在大量的NO3-,加入盐酸,在酸性条件下NO3-与金属继续反应,则剩余金属进一步溶解,以此解答.
解答 解:在Fe、Cu的混合物中加入一定量的稀硝酸并微热,充分反应后剩余金属a克,该金属可能为Fe、Cu或二者的混合物,溶液中一定存在NO3-,加入稀硫酸,在酸性条件下NO3-与金属继续反应,则剩余金属进一步溶解,则有a一定大于b,
故选D.
点评 本题考查混合物的计算,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,题目难度不大,注意NO3-在酸性条件下的性质.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.下列各项中表达正确的是( )
| A. | NaCl的电子式: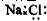 | B. | N2的结构式: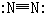 | C. | NH4Cl的电子式为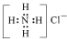 | D. | F-的结构示意图: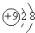 |
10.下面的排序正确的是( )
| A. | 晶体熔点由低到高:CCl4<CBr4<CI4<CF4 | |
| B. | 晶格能由大到小:NaF>NaCl>NaBr>NaI | |
| C. | 熔点由高到低:Na>Mg>Al | |
| D. | 硬度由大到小:金刚石>晶体硅>碳化硅 |
14.银锌钮扣电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为Ag2O+Zn$?_{充电}^{放电}$2Ag+ZnO,在此电池放电时,则下列说法正确的是( )
| A. | 氧化银为正极,被还原 | B. | 银为负极,被氧化 | ||
| C. | Zn为负极,被还原 | D. | 该装置中的电解质为酸性物质 |
4.有机化合物中的 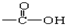 中的-OH被卤原子取代所得的化合物为酰卤,下列化合物中可以看作酰卤的是( )
中的-OH被卤原子取代所得的化合物为酰卤,下列化合物中可以看作酰卤的是( )
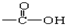 中的-OH被卤原子取代所得的化合物为酰卤,下列化合物中可以看作酰卤的是( )
中的-OH被卤原子取代所得的化合物为酰卤,下列化合物中可以看作酰卤的是( )| A. | HCOOH | B. | CCl4 | C. | COCl2 | D. | CH2ClCOOH |
11.与Ne的核外电子排布相同的离子跟与Ar的核外电子排布相同的离子所形成的化合物是( )
| A. | Na2S | B. | CCl4 | C. | KCl | D. | NaF |
8.可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极.下列说法正确的是( )
| A. | 以NaCl溶液或NaOH溶液为电解液时,正极反应都为O2+2H2O+4e-═4OH- | |
| B. | 以NaOH溶液为电解液时,负极反应为Al+3OH--3e-═Al(OH)3 | |
| C. | 以NaOH溶液为电解液时,电池在工作过程中电解液的碱性保持不变 | |
| D. | 电池工作时,当有3mol电子通过外电路时,消耗16.8LO2 |
 2SO3(g)反应,当密度保持不变,在恒温恒容或恒温恒压条件下,均不能作为达到化学平衡状态的标志
2SO3(g)反应,当密度保持不变,在恒温恒容或恒温恒压条件下,均不能作为达到化学平衡状态的标志