题目内容
按下列实验方法不能达到要求的是( )
①用500mL 容量瓶配制1mol/L NaOH溶液490mL
②用100mL量筒量取6.5mL稀硫酸
③用酚酞试液检测出某溶液的pH值为12
④用托盘天平称量5.85g NaCl.
①用500mL 容量瓶配制1mol/L NaOH溶液490mL
②用100mL量筒量取6.5mL稀硫酸
③用酚酞试液检测出某溶液的pH值为12
④用托盘天平称量5.85g NaCl.
| A、②③④ | B、①②③ |
| C、①②④ | D、①②③④ |
考点:溶液的配制,计量仪器及使用方法
专题:实验评价题
分析:①容量瓶没有具体刻度,配制490ml的氢氧化钠溶液,应该选用500mL的容量瓶;
②量取6.5mL稀硫酸时需要使用10mL量筒;
③酚酞只能指示溶液酸碱性,无法测定出溶液的具体pH数值;
④托盘天平的最小读数为0.1g,无法用托盘天平量取0.01g的氯化钠.
②量取6.5mL稀硫酸时需要使用10mL量筒;
③酚酞只能指示溶液酸碱性,无法测定出溶液的具体pH数值;
④托盘天平的最小读数为0.1g,无法用托盘天平量取0.01g的氯化钠.
解答:
解:①由于容量瓶没有具体小刻度,所以配制490mL 1mol/L 的NaOH溶液时应该选用500mL的容量瓶,故①正确;
②量取6.5mL溶液应该选用10mL的量筒,不能用100mL量筒量取6.5mL稀硫酸,否则会产生较大误差,故②错误;
③酚酞为酸碱指示剂,只能由于判断溶液酸碱性,无法用酚酞试液检测出某溶液的具体pH值数值,故③错误;
④托盘天平的最小读数为0.1g,无法用托盘天平称量5.85g NaCl,故④错误;
故选A.
②量取6.5mL溶液应该选用10mL的量筒,不能用100mL量筒量取6.5mL稀硫酸,否则会产生较大误差,故②错误;
③酚酞为酸碱指示剂,只能由于判断溶液酸碱性,无法用酚酞试液检测出某溶液的具体pH值数值,故③错误;
④托盘天平的最小读数为0.1g,无法用托盘天平称量5.85g NaCl,故④错误;
故选A.
点评:本题考查了溶液的配制、指示剂的使用方法、计量仪器的使用方法,题目难度不大,注意掌握溶液的配制方法,明确常见计量仪器的构造及使用方法.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
下列含手性碳原子的分子是( )
| A、CCl2F2 |
| B、CH3CH2OH |
| C、CH2OHCHOHCH2OH |
| D、CH3CHOHCOOH |
分子式为C6H12O2的有机物在酸性条件下可水解为酸和醇,且生成的醇没有相同官能团的同分异构体.若不考虑立体异构,这些酸和醇重新组合可形成的酯共有( )
| A、8种 | B、12种 |
| C、24种 | D、28种 |
在元素周期表中的某些元素之间存在着特殊的“对角线关系”,下列有关说法不正确的是( )
| A、氢氧化铍是两性氢氧化物 |
| B、B、Si的电负性数值相似 |
| C、Li和Mg的原子半径相近,且核外电子排布相近 |
| D、铍与盐酸或氢氧化钠溶液反应均能产生气体 |
甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合制备甲醇,该反应的热化学方程式为:
CO (g)+2H2(g)?CH3OH (g)△H1=-116kJ?mol-1某些化学键的键能数据如下表:
则CO中碳氧键的键能是( )
CO (g)+2H2(g)?CH3OH (g)△H1=-116kJ?mol-1某些化学键的键能数据如下表:
| 化学键 | C-H | H-H | C-O | H-O |
| 键能/kJ?mol-1 | 413 | 436 | 358 | 463 |
| A、431kJ?mol-1 |
| B、946kJ?mol-1 |
| C、1072kJ?mol-1 |
| D、1130kJ?mol-1 |
以下烃中,一氯代物只有一种的是( )
| A、CH3 CH2 CH2 CH2CH3 |
| B、CH3CH2CH3 |
| C、CH3CH2CH2CH3 |
| D、C(CH3)4 |
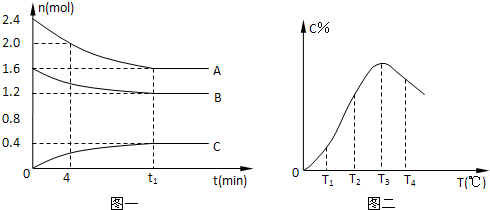
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系;当在某一温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二.
下列分析不正确的是( )

下列分析不正确的是( )
| A、0~4分钟时,A的平均反应速率为0.02mol/(L?min) | ||
B、该反应的平衡常数表达式K=
| ||
| C、由T1向T2变化时,V正>V逆 | ||
| D、此反应的正反应为吸热反应 |
下列反应中,既属于化合反应,又属于氧化还原反应的是( )
| A、2Fel2+Cl2=2FeCl3 |
| B、CaO+H2O=Ca(OH)2 |
| C、2H2O2=2H2O+O2 |
| D、Cl2+2NaBr=2NaCl+Br2 |