题目内容
下列含手性碳原子的分子是( )
| A、CCl2F2 |
| B、CH3CH2OH |
| C、CH2OHCHOHCH2OH |
| D、CH3CHOHCOOH |
考点:常见有机化合物的结构
专题:有机化学基础
分析:根据手性碳原子指连有四个不同基团的碳原子,手性碳原子判断注意:(1)手性碳原子一定是饱和碳原子;(2)手性碳原子所连接的四个基团要是不同的.
解答:
解:A、CCl2F2中碳原子所连接的四个基团有2个是一样的,该碳原子没有手性,故A错误;
B、CH3CH2OH中一个碳原子所连接的四个基团有3个是一样的,另一个碳原子所连接的四个基团有2个是一样的,碳原子没有手性,故B错误;
C、CH2OHCHOHCH2OH中连接的四个基团有2个是一样的,该碳原子没有手性,故C错误;
D、CH3CHOHCOOH中间的碳原子连有的四个不同取代基,该碳原子具有手性,故D正确;
故选D.
B、CH3CH2OH中一个碳原子所连接的四个基团有3个是一样的,另一个碳原子所连接的四个基团有2个是一样的,碳原子没有手性,故B错误;
C、CH2OHCHOHCH2OH中连接的四个基团有2个是一样的,该碳原子没有手性,故C错误;
D、CH3CHOHCOOH中间的碳原子连有的四个不同取代基,该碳原子具有手性,故D正确;
故选D.
点评:本题主要考查手性碳原子的判断,手性碳原子判断注意:手性碳原子一定是饱和碳原子,手性碳原子所连接的四个基团要是不同的.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
以乙炔作为原料的合成反应,下列过程中能生成CH2BrCHBrCl的是( )
| A、先加HCl,再加HBr |
| B、先加Cl2再加HBr |
| C、先加HCl,再加Br2 |
| D、先加HBr,再加HCl |
已知在相同状况下,同一化学键断裂需要吸收的能量等于形成该化学键放出的能量.下列说法错误的是( )
| A、电解熔融的Al2O3可以制得金属铝和氧气,该反应是一个放出能量的反应 |
| B、H2(g)+F2(g)=2HF(g)△H=-270 kJ/mol,1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270 kJ热量 |
| C、相同状况下,反应2SO2+O2=2SO3是一个放热反应,则反应2SO3=2SO2+O2是一个吸热反应 |
| D、破坏1 mol氢气中的化学键消耗的能量为Q1 kJ,破坏1 mol氯气中的化学键消耗的能量为Q2 kJ,形成1 mol氯化氢中的化学键释放的能量为Q3 kJ,则Q1+Q2<2Q3 |
下列离子方程式正确的是( )
| A、钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ | ||
| B、AlCl3溶液中加入过量的浓氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ | ||
C、用小苏打治疗胃酸过多:CO
| ||
| D、用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+ |
下列关于氮的叙述中正确的是( )
| A、氮分子为极性分子 |
| B、氮气的性质活泼,在常温下能与H2、O2等非金属反应 |
| C、液氮可作制冷 |
| D、氮有多种化合价 |
按下列实验方法不能达到要求的是( )
①用500mL 容量瓶配制1mol/L NaOH溶液490mL
②用100mL量筒量取6.5mL稀硫酸
③用酚酞试液检测出某溶液的pH值为12
④用托盘天平称量5.85g NaCl.
①用500mL 容量瓶配制1mol/L NaOH溶液490mL
②用100mL量筒量取6.5mL稀硫酸
③用酚酞试液检测出某溶液的pH值为12
④用托盘天平称量5.85g NaCl.
| A、②③④ | B、①②③ |
| C、①②④ | D、①②③④ |
 25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法正确的是( )
25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法正确的是( )| A、在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX | ||
| B、根据滴定曲线,可得Ka(HY)≈10-5 | ||
| C、将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+) | ||
D、HY与HZ混合,达到平衡时:c(H+)=
|
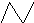 ,有机物A的键线式结构为
,有机物A的键线式结构为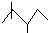 ,有机物B与等物质的量的H2发生加成反应可得到有机物A.则:
,有机物B与等物质的量的H2发生加成反应可得到有机物A.则: