题目内容
14.已知aAn+,bB(n+1)+,cCn-,dD(n+1)-是具有相同的电子层结构的短周期元素形成的简单离子,下列叙述正确的是( )| A. | 原子半径:C>D>A>B | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:Cn+>D(n+)->An+>B(n+)+ | D. | 单质还原性:A>B>C>D |
分析 aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,则有:a-n=b-(n+1)=c+n=d+(n+1),原子序数:b>a>c>d,A、B同周期,C、D同周期,且A、B在周期表中C、D的下一周期,由形成的离子可知,A、B为金属,C、D为非金属性,结合元素周期律递变规律解答该题.
解答 解:aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,则有:a-n=b-(n+1)=c+n=d+(n+1),原子序数:b>a>c>d,A、B同周期,C、D同周期,且A、B在周期表中C、D的下一周期,四种元素的相对位置: ,则
,则
A.A、B在周期表中C、D的下一周期,并且原子序数:b>a>c>d,原子核外电子层数越多,原子半径越大,同周期元素原子序数越大,原子半径越小,则有原子半径:A>B>D>C,故A错误;
B.aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,则有:a-n=b-(n+1)=c+n=d+(n+1),则有原子序数:b>a>c>d,故B正确;
C.aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,核电荷数越大离子半径越小,核电荷数b>a>c>d,故离子半径dD(n+1)->cCn->aAn+>bB(n+1),故C错误;
D.A、B在周期表中同周期,原子序数:b>a,金属性:A>B,对应单质的还原性:A>B,C、D在周期表同周期,原子序数c>d,非金属性C>D,对应单质的氧化性C>D,所以还原性C<D,故D错误,
故选B.
点评 本题考查位置结构性质关系及应用,根据核外电子排布确定元素所在周期表中的位置以及把握元素周期律的递变规律是解答该题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.酯R在稀硫酸,加热的条件下可生成1molHOCH2CH2OH(乙二醇)和2mol羧酸(C5H10O2),则R的结构有( )
| A. | 6种 | B. | 10种 | C. | 12种 | D. | 14种 |
2.下列原子中未成对电子(单独占据1个原子轨道的电子)数为2的是( )
| A. | O | B. | N | C. | Cu | D. | F |
9.下列解释过程或事实的方程式不正确的是( )
| A. | Na放入水中,产生气体:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 液氨作为清洁能源的反应原理是:4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O | |
| C. | NaOH溶液不能保存在玻璃塞的试剂瓶中:SiO2+2OH-═SiO32-+H2O | |
| D. | 红热的铁丝与水蒸汽接触,表面形成蓝黑色(或黑色)保护层:3Fe+4H2O(气)$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2 |
19.下列说法正确的是( )
| A. | 可用丁达尔现象区分溶液与胶体 | |
| B. | 化学变化能够实现一种原子变为另一种原子 | |
| C. | O3是由3个氧原子构成的化合物 | |
| D. | CuSO4•5H2O是一种混合物 |
6.发射航天火箭常用肼(N2H4)与N2O4作燃料与助燃刹.
(1)肼易溶于水,它是与氨类似的弱碱,用电离方程式表示肼的水溶液显碱性的原因N2H4+H2O?N2H+5+OH-.
(2)已知:2N2H4 (1)+N2O4 (1)═3N2(g)+4H2O(1)△H=-1225kJ•mol-1
断开1mol下列化学键吸收的能量分别为:N-H:390kJ N-N:190kJ N≡N:946kJ O-H:460kJ.
则使1mol N2O4 (1)分子中化学键完全断裂时需要吸收的能量是1793kJ
(3)已知N2O4 (1)?2NO2(g)△H=+57.20kJ•mol-1,t℃时,将一定量的NO2、N2O4充入一个容积为2L的恒容密闭容器中,浓度随时间变化关系如表所示:
①c(X)代表NO2(填化学式)的浓度,该反应的平衡常数K=0.9;
②前10min内用NO2表示的反应速率为0.04mol/(L.min),20min时改变的条件是增大NO2的浓度;重新达到平衡时,NO2的百分含量b(填序号)
a.增大 b.减小 C.不变 d.无法判断
(4)已知:在相同条件下N2H4•H2O的电离程度大于N2H5C1的水解程度.常温下,若将0.2mo1•L-1N2H4•H2O溶液与0.1mol•L-1HCl溶液等体积混合,则溶液中N2H5+、Cl-、OH-、H+离子浓度由大到小的顺序为c(N2H5+)>c(Cl-)>c(OH-)>c(H+).
(1)肼易溶于水,它是与氨类似的弱碱,用电离方程式表示肼的水溶液显碱性的原因N2H4+H2O?N2H+5+OH-.
(2)已知:2N2H4 (1)+N2O4 (1)═3N2(g)+4H2O(1)△H=-1225kJ•mol-1
断开1mol下列化学键吸收的能量分别为:N-H:390kJ N-N:190kJ N≡N:946kJ O-H:460kJ.
则使1mol N2O4 (1)分子中化学键完全断裂时需要吸收的能量是1793kJ
(3)已知N2O4 (1)?2NO2(g)△H=+57.20kJ•mol-1,t℃时,将一定量的NO2、N2O4充入一个容积为2L的恒容密闭容器中,浓度随时间变化关系如表所示:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c(X)/mol•L-1 | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c(YX)/mol•L-1 | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
②前10min内用NO2表示的反应速率为0.04mol/(L.min),20min时改变的条件是增大NO2的浓度;重新达到平衡时,NO2的百分含量b(填序号)
a.增大 b.减小 C.不变 d.无法判断
(4)已知:在相同条件下N2H4•H2O的电离程度大于N2H5C1的水解程度.常温下,若将0.2mo1•L-1N2H4•H2O溶液与0.1mol•L-1HCl溶液等体积混合,则溶液中N2H5+、Cl-、OH-、H+离子浓度由大到小的顺序为c(N2H5+)>c(Cl-)>c(OH-)>c(H+).
4.电镀工业会产生大量的电镀污水,处理电镀污水时会产生大量的电镀污泥.电镀污泥含.有多种金属氢氧化物和杂质.下面是处理某种电镀污泥回收铜、镍元素的一种工业流程.
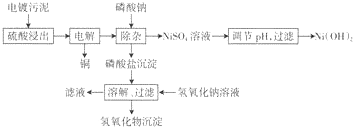
电镀污泥用硫酸浸出后得到的浸出液中各金属离子浓度见下表.
(1)硫酸浸出过程中,为提高浸出速率,可以采取的措施有加热、增大硫酸浓度、搅拌(写出两条).
(2)在电解回收铜的过程中,为提高下一步的除杂效果,需控制电解电压稍大一些使Fe2+氧化,则磷酸盐沉淀中含有的物质为FePO4、CrPO4、AlPO4.
(3)假设电解前后Ni2+浓度基本不变,若使Ni2+在除杂过程不损失,则溶液中P043-浓度不能超过$\sqrt{\frac{5×1{0}^{-31}}{(\frac{7}{59})^{3}}}$mol.L-l.(列出计算表达式,Ksp[Ni3(P04)2]=5xl0-31)
(4)滤液中的Na3PO4可回收循环使用;研究发现当NaOH溶液浓度过大时,部分铝元素和铬元素会在滤液中出现,滤液中出现铝元素的原因为Al(OH)3+OH-=AlO2-+2H2O(用离子方程式解释).
(5)Ni(OH)2是镍氢蓄电池的正极材料,在碱性电解质中,电池充电时Ni(OH)2变为NiOOH,则电池放电时正极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-.
(6)电镀污水中的Cr元素也可以用铁氧体法处理,原理为在废水中加入过量的FeS04,在酸性条件下Cr2072-被还原为Cr3+,同时生成Fe3+;再加入过量的强碱生成铁铬氧体(CrxFe3-xO4)沉淀.写出加入过量强碱生成铁铬氧体( CrxFe3-xO4)沉淀的离子方程式xCr3++Fe2++(2-x)Fe3++8OH-=CrxFe3-xO4↓+4H2O.

电镀污泥用硫酸浸出后得到的浸出液中各金属离子浓度见下表.
| 金属离子 | Cu3+ | Ni3+ | Fe3+ | Al3+ | Cr3+ |
| 浓度(mg/L) | 7000 | 7000 | 2500 | 4200 | 3500 |
(2)在电解回收铜的过程中,为提高下一步的除杂效果,需控制电解电压稍大一些使Fe2+氧化,则磷酸盐沉淀中含有的物质为FePO4、CrPO4、AlPO4.
(3)假设电解前后Ni2+浓度基本不变,若使Ni2+在除杂过程不损失,则溶液中P043-浓度不能超过$\sqrt{\frac{5×1{0}^{-31}}{(\frac{7}{59})^{3}}}$mol.L-l.(列出计算表达式,Ksp[Ni3(P04)2]=5xl0-31)
(4)滤液中的Na3PO4可回收循环使用;研究发现当NaOH溶液浓度过大时,部分铝元素和铬元素会在滤液中出现,滤液中出现铝元素的原因为Al(OH)3+OH-=AlO2-+2H2O(用离子方程式解释).
(5)Ni(OH)2是镍氢蓄电池的正极材料,在碱性电解质中,电池充电时Ni(OH)2变为NiOOH,则电池放电时正极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-.
(6)电镀污水中的Cr元素也可以用铁氧体法处理,原理为在废水中加入过量的FeS04,在酸性条件下Cr2072-被还原为Cr3+,同时生成Fe3+;再加入过量的强碱生成铁铬氧体(CrxFe3-xO4)沉淀.写出加入过量强碱生成铁铬氧体( CrxFe3-xO4)沉淀的离子方程式xCr3++Fe2++(2-x)Fe3++8OH-=CrxFe3-xO4↓+4H2O.
 .
.