题目内容
据悉,奥运会上使用的发令枪所用的“火药”成分是氯酸钾和红磷,经撞击发出响同时产生白色烟雾.撞击时发生的化学方程式为:5KC1O3+6P═3P2O5+5KC1,下列有关叙述正确的是( )
| A、上述反应中氧化剂和还原剂的物质的量之比为6:5 |
| B、产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾) |
| C、上述反应中消耗2molP时,转移电子的物质的量为15mol |
| D、因红磷和白磷互为同位素,所以上述火药中的红磷可以用白磷代替 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:该反应中Cl元素化合价由+5价变为-1价、P元素化合价由0价变为+5价,
A.根据元素化合价知,氯酸钾是氧化剂、P是还原剂;
B.P2O5是白色固体颗粒,且P2O5具有吸水性,能吸收水分形成酸的小液滴;
C.根据元素化合价变化计算转移电子物质的量;
D.白磷熔点较低,易自燃.
A.根据元素化合价知,氯酸钾是氧化剂、P是还原剂;
B.P2O5是白色固体颗粒,且P2O5具有吸水性,能吸收水分形成酸的小液滴;
C.根据元素化合价变化计算转移电子物质的量;
D.白磷熔点较低,易自燃.
解答:
解:该反应中Cl元素化合价由+5价变为-1价、P元素化合价由0价变为+5价,
A.根据元素化合价知,氯酸钾是氧化剂、P是还原剂,所以氧化剂和还原剂的物质的量之比为5:6,故A错误;
B.P2O5是白色固体颗粒,且P2O5具有吸水性,能吸收水分形成酸的小液滴,固体颗粒为烟、小液滴为雾,所以产生烟雾,故B正确;
C.上述反应中消耗2molP时,转移电子的物质的量=2mol×(5-0)=10mol,故C错误;
D.白磷熔点较低,易自燃,会造成安全隐患,故D错误;
故选B.
A.根据元素化合价知,氯酸钾是氧化剂、P是还原剂,所以氧化剂和还原剂的物质的量之比为5:6,故A错误;
B.P2O5是白色固体颗粒,且P2O5具有吸水性,能吸收水分形成酸的小液滴,固体颗粒为烟、小液滴为雾,所以产生烟雾,故B正确;
C.上述反应中消耗2molP时,转移电子的物质的量=2mol×(5-0)=10mol,故C错误;
D.白磷熔点较低,易自燃,会造成安全隐患,故D错误;
故选B.
点评:本题考查氧化还原反应,侧重考查基本概念、计算,明确元素化合价变化是解本题关键,知道白磷、红磷性质的区别,题目难度不大.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的密闭容器中,发生反应:2SO2+O2?2SO3,平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是( )
| A、2 mol SO2+1 mol O2 |
| B、4 mol SO2+1 mol O2 |
| C、2 mol SO2+1 mol O2+2 SO3 |
| D、3 mol SO2+0.5 mol O2+1 SO3 |
下列叙述正确的是( )
| A、金属单质与盐溶液的反应都是置换反应 |
| B、加碘食盐中添加碘酸钾而不用碘化钾,是因为碘酸钾能溶于水而碘化钾难溶于水 |
| C、与强酸、强碱都反应的物质只有两性氧化物和两性氢氧化物 |
| D、氯气可用作消毒剂和漂白剂,是因为氯气与水反应生成的次氯酸具有强氧化性 |
下列事实与氢键无关的是( )
| A、氨和水反应生成NH3?H2O |
| B、DNA双螺旋结构 |
| C、水在高温下分解成氢气和氧气 |
| D、乙醇比二甲醚易溶于水 |
下列说法正确的是( )
| A、NaCl固体中含有共价键 | ||||||
| B、CO2分子中含有离子键 | ||||||
C、
| ||||||
D、
|
下列各式中正确表示电解质电离的是( )
| A、H3PO4?T3H++PO43- |
| B、HCO3-+H2O?H3O++CO32- |
| C、CH3COONH4?CH3COO-+NH4+ |
| D、NaHS═Na++H++S2- |
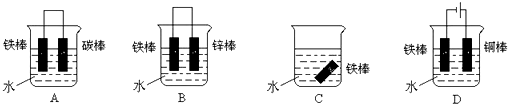
 三个课外实验小组用Na2SO3溶液、FeCl3溶液及其它试剂做了一系列实验:
三个课外实验小组用Na2SO3溶液、FeCl3溶液及其它试剂做了一系列实验: