题目内容
14. 在一定固定容积的密闭容器中,CO2(g)与一定量的C(s)发生进行如下化学反应:CO2(g)+C(s)?2CO(g).
在一定固定容积的密闭容器中,CO2(g)与一定量的C(s)发生进行如下化学反应:CO2(g)+C(s)?2CO(g).①该反应为吸热反应(填“吸热”或“放热”).
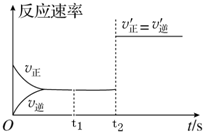
②该反应的反应速率随时间的变化图象如图所示,则下列说法正确的是ac(填序号).
a.t1时刻该反应已经处于化学平衡状态
b.t2时刻c(CO2)=c(CO)
c.t2时刻该反应仍然处于化学平衡状态
d.t2时刻,改变的条件可能是增大了C的物质的量.
分析 ①CO2(g)与一定量的C(s)发生的反应是吸热反应;
②a.t1时刻正逆反应速率相同;
b.t2时刻改变条件正逆反应速率不变,依据起始量和变化量可知不能确定c(CO2)=c(CO);
c.t2时刻改变条件后正逆反应速率增大,是同等程度增大,平衡不变;
d.t2时刻若增大了C的物质的量,碳为固体不影响化学平衡,也不影响化学反应速率.
解答 解:①CO2(g)与一定量的C(s)发生的反应,CO2(g)+C(s)?2CO(g).该反应是常见的化合反应中的吸热反应,所以反应是吸热反应,
故答案为:吸热;
②a.t1时刻正逆反应速率相同,是平衡的标志,反应达到平衡状态,故a正确;
b.t2时刻改变条件正逆反应速率不变,起始量和变化量决定平衡后的浓度关系,不能确定c(CO2)=c(CO),故b错误;
c.t2时刻改变条件后正逆反应速率增大,但是正逆反应速率同等程度增大,平衡不变,t2时刻该反应仍然处于化学平衡状态,故c正确;
d.t2时刻若增大了C的物质的量,碳为固体不影响化学平衡,也不影响化学反应速率,不符合图象中正逆反应速率都增大,故d错误.
故答案为:ac.
点评 本题考查了化学平衡的建立、影响反应速率和平衡状态的因素分析判断,注意固体不影响反应速率和化学平衡,题目难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
2.设阿伏伽德罗常数的值为NA,则下列说法正确的是( )
| A. | 标准状况下,11.2LCCl4所含的分子数为0.5NA | |
| B. | 7.8g苯分子中碳碳双键的数目为0.3NA | |
| C. | 常温常压下,4.2gC2H4和C9H18混合物中含有的碳原子数为0.3NA | |
| D. | 常温下,1molC3H8含有C-H共价键数为10NA |
2.下列化学式仅代表一种物质的是( )
| A. | CH4O | B. | C3H8O | C. | C3H6 | D. | C2H4O2 |
3.化学与生活密切相关,下列生活现象中没有发生化学变化的是( )
| A. | 夜晚霓虹灯放出五颜六色的光 | B. | 漂白粉消毒 | ||
| C. | 明矾净水 | D. | 二氧化硫熏蒸银耳 |
4.下列说法正确的是( )
| A. | SiH4比CH4稳定 | |
| B. | O2-半径比F-的大 | |
| C. | Na和Cs属于第 IA族元素,Cs失电子能力比Na弱 | |
| D. | P和As属于第 VA族元素,H3PO4酸性比H3AsO4弱 |
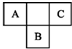 A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.
A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等. ,C的氢化物与B的氢化物的稳定性强弱顺序为HF>H2S(填化学式).
,C的氢化物与B的氢化物的稳定性强弱顺序为HF>H2S(填化学式).