题目内容
13.下列说法正确的是( )| A. | 第一电离能:Al>Mg | B. | 水溶性:CH3CH2OH>CH3CH2OCH2CH3 | ||
| C. | 沸点:HCl>HF | D. | 晶格能:NaCl>MgO |
分析 A.同一主族元素,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族第一电离能大于其相邻元素;
B.有机物的溶解性:醇>醚;
C.含有氢键的氢化物熔沸点较高;
D.离子化合物中晶格能与电荷成正比、与离子半径成反比.
解答 解:A.同一主族元素,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族第一电离能大于其相邻元素,所以第一电离能Mg>Al,故A错误;
B.有机物的溶解性:醇>醚,所以溶解性CH3CH2OH>CH3CH2OCH2CH3,故B正确;
C.含有氢键的氢化物熔沸点较高,HF中含有氢键、HCl中不含氢键,所以熔沸点HF>HCl,故C错误;
D.离子化合物中晶格能与电荷成正比、与离子半径成反比,镁离子和氧离子电荷大于钠离子和锂离子,所以晶格能MgO>NaCl,故D错误;
故选B.
点评 本题考查元素周期律、晶格能、熔沸点等知识点,为高频考点,明确元素周期律、物质结构和性质的关系是解本题关键,注意氢化物的稳定性与化学键有关、氢化物的熔沸点与分子间作用力有关,为易错点.

练习册系列答案
相关题目
4.铜锌原电池(如图)工作时,下列叙述正确的是( )
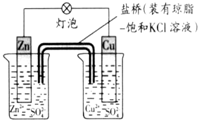

| A. | 正极反应为:Zn-2e-=Zn2+ | B. | Cu为负极,发生还原反应 | ||
| C. | 盐桥中的K+移向ZnSO4溶液 | D. | 在外电路中,电子从负极流向正极 |
1.海洋资源的开发与利用具有广阔的前景.海水的pH一般在7.5~8.6之间.某地海水中主要离子的含量如表:
(1)海水显弱碱性的原因是(用离子方程式表示):HCO3-+H2O?H2CO3+OH-,该海水中Ca2+的物质的量浓度为5×10-3 mol/L.
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如如图1所示.其中阴(阳)离子交换膜只允许
阴(阳)离子通过.
①阴极的电极反应式为2H++2e-=H2↑.
②电解一段时间,阴极区会产生水垢,其成分为CaCO3和Mg(OH)2,写出生成CaCO3的离子方程式Ca2++OH-+HCO3-=CaCO3↓+H2O.
③淡水的出口为a、b、c中的b出口.
(3)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力.锂是制造化学电源的重要原料,如LiFePO4电池某电极的工
作原理如图2所示:
该电池的电解质是能传导 Li+的固体材料.
则放电时该电极是电池的正极(填“正”或“负”),电极反应式为FePO4+e-+Li+=LiFePO4.
(4)利用海洋资源可获得MnO2.MnO2可用来制备高锰酸钾:将MnO2与KOH混合后在空气中加热熔融,得到绿色的锰酸钾(K2MnO4),再利用氯气将锰酸钾氧化成高锰酸钾.该制备过程中消耗相同条件下空气和氯气的体积比为5:1(空气中氧气的体积分数按20%计).

| 成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | SO42- | HCO3- |
| 含量/mg?L-1 | 9360 | 83 | 200 | 1100 | 16000 | 1200 | 118 |
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如如图1所示.其中阴(阳)离子交换膜只允许
阴(阳)离子通过.
①阴极的电极反应式为2H++2e-=H2↑.
②电解一段时间,阴极区会产生水垢,其成分为CaCO3和Mg(OH)2,写出生成CaCO3的离子方程式Ca2++OH-+HCO3-=CaCO3↓+H2O.
③淡水的出口为a、b、c中的b出口.
(3)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力.锂是制造化学电源的重要原料,如LiFePO4电池某电极的工
作原理如图2所示:
该电池的电解质是能传导 Li+的固体材料.
则放电时该电极是电池的正极(填“正”或“负”),电极反应式为FePO4+e-+Li+=LiFePO4.
(4)利用海洋资源可获得MnO2.MnO2可用来制备高锰酸钾:将MnO2与KOH混合后在空气中加热熔融,得到绿色的锰酸钾(K2MnO4),再利用氯气将锰酸钾氧化成高锰酸钾.该制备过程中消耗相同条件下空气和氯气的体积比为5:1(空气中氧气的体积分数按20%计).

8.下列实验现象的叙述,正确的是( )
| A. | 钠在氧气中燃烧,火焰呈黄色,产生白色固体 | |
| B. | 红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 | |
| C. | 氢气在氯气中燃烧,发出苍白色火焰,同时产生白烟 | |
| D. | 钠投入水中,将沉在水底并熔化成小球,且有气泡产生 |
18.下列说法正确的是( )
| A. | 化学反应不一定伴随着能量的变化 | |
| B. | 氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=571.6kJ•mol-1 | |
| C. | 放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关D.所有燃烧反应都是放热反应,所以不需吸收能量就可以进行 | |
| D. | 所有燃烧反应都是放热反应,所以不需吸收能量就可以进行 |
5.用脱脂棉包住约0.2gNa2O2粉末,投入盛满CO2的集气瓶中,棉花燃烧,此实验不能得出的结论是( )
| A. | CO2在一定条件下可以支持燃烧 | B. | 该反应是一个放热反应 | ||
| C. | 该实验的反应中有O2生成 | D. | Na2O2可作为呼吸面具中氧气来源 |
2.下列化合物既能通过单质间的化合反应制得,又能通过单质和稀盐酸反应制得的是( )
| A. | FeCl2 | B. | CuCl2 | C. | AlCl3 | D. | FeCl3 |
 一定温度下,某容积为2L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图所示:
一定温度下,某容积为2L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图所示: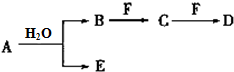 A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题:
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题: ;D中所含化学键的类型离子键、共价键.
;D中所含化学键的类型离子键、共价键.