题目内容
10.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )| A. | 标准状况下,33.6LCHCl3的分子数为1.5NA | |
| B. | 4.6g乙醇含极性共价键的数目为0.8NA | |
| C. | 4.2g由C2H4和C4H8组成的混合物中含碳原子的数目为0.3NA | |
| D. | 1L0.1mol•L-1的醋酸溶液中含H+数为0.1NA |
分析 A、标况下三氯甲烷为液态;
B、求出乙醇的物质的量,然后根据乙醇中含7条极性键来分析;
C、C2H4和C4H8的最简式均为CH2;
D、醋酸是弱电解质,在溶液中不能完全电离.
解答 解:A、标况下三氯甲烷为液态,故不能根据气体摩尔体积来计算其物质的量和分子个数,故A错误;
B、4.6g乙醇的物质的量为n=$\frac{4.6g}{46g/mol}$=0.1mol,而乙醇中含5条C-H键、1条C-O键和1条O-H键即共7条极性键,故0.1mol乙醇中含有极性键为0.7NA条,故B错误;
C、C2H4和C4H8的最简式均为CH2,故4.2g混合物中含有的CH2的物质的量为0.3mol,则含0.3NA个碳原子,故C正确;
D、醋酸是弱电解质,在溶液中不能完全电离,故溶液中的氢离子的个数小于0.1NA个,故D错误.
故选C.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.

练习册系列答案
相关题目
20.下列说法不正确的是( )
| A. | 植物油能使溴的四氯化碳溶液褪色 | |
| B. | 蛋白质、纤维素、油脂、淀粉都是高分子化合物 | |
| C. | 石油裂化、煤的干馏、铝热反应都属于化学变化 | |
| D. | 乙烯常用作水果催熟剂,乙酸常用作调味剂,乙醇常用于杀菌消毒 |
1.化学与生活密切相关,下列有关说法错误的是( )
| A. | 油脂和蛋白质都属于高分子化合物 | |
| B. | 乙醇室温下在水中的溶解度大于溴乙烷 | |
| C. | 以液化石油气代替燃油可减少大气污染 | |
| D. | “地沟油”禁止食用,但可以用来制皂 |
18.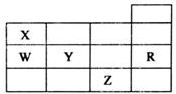 五种前四周期元素X、Y、Z、W、R在元素周期表中的位置如图所示.下列有关元素的叙述中,正确的是( )
五种前四周期元素X、Y、Z、W、R在元素周期表中的位置如图所示.下列有关元素的叙述中,正确的是( )
 五种前四周期元素X、Y、Z、W、R在元素周期表中的位置如图所示.下列有关元素的叙述中,正确的是( )
五种前四周期元素X、Y、Z、W、R在元素周期表中的位置如图所示.下列有关元素的叙述中,正确的是( )| A. | W的简单氢化物的沸点比X的简单氢化物的沸点低 | |
| B. | 五种元素均在元素周期表的s区 | |
| C. | 电负性和第一电离能均为:Y>X>W | |
| D. | 五种元素的单质所形成的晶体类型不相同 |
5.下列有关说法正确的是( )
| A. | 蛋白质和油脂都属于高分子化合物,一定条件下都能水解 | |
| B. | 医疗上可用硫酸钡作x射线透视肠胃的内服药,是因为硫酸钡不溶于水 | |
| C. | 用过滤的方法从碘的四氯化碳溶液中获得碘 | |
| D. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
15.用NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A. | 1molCu和足量热浓硫酸反应可生成NA个SO3分子 | |
| B. | 3mol单质Fe与足量水蒸气完全反应,失去9NA个电子 | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 22.4L的Cl2与足量水反应,转移电子数为1NA |
2.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 1mol氯气与足量水反应时转移的电子数为NA | |
| B. | 18g D2O中含有10NA个电子 | |
| C. | 50mL 18.4mol•L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA | |
| D. | 1mol氯气与过量铁反应时转移的电子数为2NA |
8.“绿色化学”是当今社会提出的一个新概念.在“绿色化学工艺”中,理想状态是反应物中原子全部为欲制得的产物,即原子利用率为100%.在用CH3C≡CH合成CH2=C(CH3) COOCH3的过程中,欲使原子利用率达到最高,还需要其他的反应物有( )
| A. | CO和CH3OH | B. | CO2和 H2O | C. | H2和CO2 | D. | CH3OH和H2 |
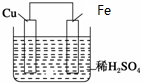 如图是Fe和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )
如图是Fe和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )