题目内容
18.请回答下列问题:(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:
CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+260kJ•mol-1
已知:2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1
则CH4与O2反应生成CO和H2的热化学方程式为2CH4(g)+O2(g)=2CO(g)+4H2(g)△H=-46kJ•mol-1;
(2)钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的1/4.
钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式.
正极:O2+2H2O+4e-=4OH-;负极:Fe-2e-=Fe2+.
分析 (1)已知:①CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+260kJ•mol-1,
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1,
根据盖斯定律①×2+②可得;
(2)钢铁发生吸氧腐蚀,负极上Fe失电子发生氧化反应,正极上氧气得电子发生还原反应.
解答 解:(1)已知:①CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+260kJ•mol-1,
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1,
根据盖斯定律①×2+②可得:2CH4(g)+O2(g)=2CO(g)+4H2(g)△H=-46kJ•mol-1;
故答案为:2CH4(g)+O2(g)=2CO(g)+4H2(g)△H=-46kJ•mol-1;
(2)钢铁发生吸氧腐蚀,正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-=4OH-,负极上Fe失电子发生氧化反应,电极反应式为Fe-2e-=Fe2+,
故答案为:正极:O2+2H2O+4e-=4OH-;负极:Fe-2e-=Fe2+.
点评 本题考查了盖斯定律和金属的吸氧腐蚀,题目较简单,有利于学生巩固基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.相同温度下,体积相同的两个容器中,充入等质量CO2和CO气体,下列判断正确的是( )
| A. | CO2和CO对容器产生的压强之比是7:11 | |
| B. | CO2和CO的密度之比是11:7 | |
| C. | CO2和CO的分子数相等 | |
| D. | CO2和CO的氧原子个数比是22:7 |
9.已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O.每有1mol Cu(IO3)2参加反应时( )
| A. | 有12 mol KI 被氧化 | B. | 转移11 mol电子 | ||
| C. | 生成CuI 382g | D. | I2只是氧化产物 |
13.下列事实可用勒沙特列原理解释的是( )
| A. | 新制的氯水在光照条件下颜色变浅 | |
| B. | H2、I2、HI平衡混合气体加压后颜色变深 | |
| C. | 钢铁在潮湿的空气中容易生锈 | |
| D. | 加入催化剂有利于氨催化氧化的反应 |
3.向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素.下列说法正确的是( )
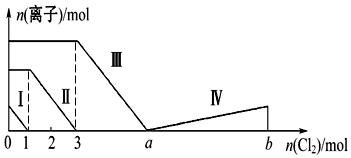

| A. | 线段Ⅱ表示Br-的变化情况 | B. | 原溶液中n(FeBr2):n(FeI2)=1:3 | ||
| C. | 线段Ⅳ表示IO3-的变化情况 | D. | 根据图象无法计算a的值 |
10.下列各选项中,正确的是( )
| A. | 实验室要配制0.lmol/LNaOH溶液400mL,需称取NaOH 固体1.6g | |
| B. | 焰火的五彩缤纷是某些金属元素化学性质的展现 | |
| C. | Al2O3熔点很高,可用作耐火材料 | |
| D. | 纯锌和铁相连接后,插入同一稀盐酸中,锌极上发生氧化还原反应 |
7.设一个碳12C的原子的质量为m g,一个R原子的质量为z g,阿伏伽德罗常数为NA,则R的相对原子质量可表示为( )
| A. | $\frac{z}{12m}$ | B. | $\frac{12z}{m}$ | C. | $\frac{{N}_{A}}{m}$ | D. | $\frac{{N}_{A}}{z}$ |