题目内容
19.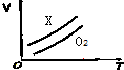 如图表示ag O2与a gX气体在恒压条件下的密闭容器中体积(V)与温度(T)的关系,则X气体可能是( )
如图表示ag O2与a gX气体在恒压条件下的密闭容器中体积(V)与温度(T)的关系,则X气体可能是( )| A. | C3H6(气) | B. | CH4 | C. | CO2 | D. | NO |
分析 同温同压下,气体体积与物质的量成正比,根据图象知,相同温度下氧气体积小于X气体的,说明氧气的物质的量小,根据n=$\frac{m}{M}$判断X摩尔质量相对大小.
解答 解:同温同压下,气体体积与物质的量成正比,根据图象知,相同温度下氧气体积小于X气体的,说明氧气的物质的量小,根据n=$\frac{m}{M}$可知,质量相同时,物质的量与摩尔质量成反比,则氧气的摩尔质量大于X的,选项中甲烷、NO的摩尔质量小于氧气的,
故选:BD.
点评 本题考查阿伏伽德罗定律及其推论,题目难度不大,注意根据PV=nRT理解阿伏伽德罗定律及其推论,掌握以物质的量为中心的计算.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.下列有关物质的分类正确的是( )
| A. | 混合物:空气、矿泉水、水银 | B. | 碱:Ba(OH)2、Cu2(OH)2CO3、NH3•H2O | ||
| C. | 氧化物:H2O、CO、HCOOH | D. | 盐:苏打 醋酸钠、氯化铵 |
10.海水开发利用的部分过程如图所示.下列说法错误的是( )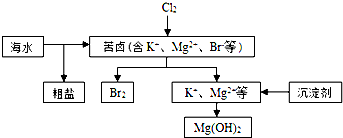

| A. | 向苦卤中通入Cl2是为了提取溴 | |
| B. | 粗盐可采用除杂和重结晶等过程提纯 | |
| C. | 富集溴一般先用空气和水蒸气吹出单质溴,在用SO2将其还原吸收 | |
| D. | 工业生产中常选用NaOH作为沉淀剂 |
7.下列离子方程式书写正确的是 ( )
| A. | Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| B. | 向NaClO溶液中通入少量SO2:2ClO-+SO2+H2O═2HClO+SO32- | |
| C. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 向NaHSO4溶液中滴加Ba(OH)2溶液至呈中性:2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓ |
4.为了探究FeS04和Cu(N03)2的混合物中各组分的含量,现设计如下流程.下列叙述中错误的是( ) 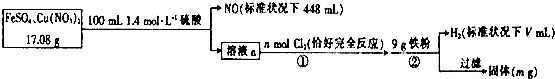

| A. | V=2240 | |
| B. | n=0.02 | |
| C. | 原混合物中FeS04的质量分数约为89% | |
| D. | m=0.6 |
11.为鉴别K2CO3和NaHCO3两种白色固体,有4位同学分别设计了不同的方法,其中不可行的是( )
| A. | 将少量的两种白色固体分别加入1 mol/L的盐酸中,看有无气泡产生 | |
| B. | 分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊 | |
| C. | 分别取样配成溶液,滴加BaCl2溶液,观察有无白色沉淀 | |
| D. | 分别配成溶液,用铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色 |
8.电子工业制造光电管时,需要一种强光照射就失电子,从而接通电路的材料,制造该材料的物质是( )
| A. | 放射元素 | B. | ⅦA族元素 | C. | 卤化银 | D. | ⅠA族元素 |
9.常温下,某溶液中水电离产生的H+浓度为1×10-9 mol•L-1,则该溶液中含有的溶质( )
| A. | 只能是酸 | B. | 只能是碱 | ||
| C. | 可能是酸也可能是碱 | D. | 只能是盐 |
