题目内容
8.电子工业制造光电管时,需要一种强光照射就失电子,从而接通电路的材料,制造该材料的物质是( )| A. | 放射元素 | B. | ⅦA族元素 | C. | 卤化银 | D. | ⅠA族元素 |
分析 根据金属活动顺序表和原子失电子的难易程度方面来分析,找原子半径最大,最外层电子最少,最容易失去电子的元素.
解答 解:根据题意,金属的原子应该是一种经强光照射就失去电子的金属原子,要求金属的活泼性相当强,极易失去电子,
A、放射元素不一定容易失电子,不符合题意,故A不选;
B、ⅦA族元素在同周期元素中原子半径小,得电子能力强,故B不选;
C、卤化银见光易分解,生成卤素单质和Ag,二者不易失电子,不符合,故C不选;
D、ⅠA族元素在同周期元素中原子半径最大,最外层电子最少,最容易失去电子的元素,故D选.
故选D.
点评 本题考查了元素的性质及应用,侧重于考查学生根据题目信息结合金属活动顺序表来分析解决问题的能力,题目难度不大.

练习册系列答案
相关题目
18.液态锂离子电池充放电时总反应可表示为:
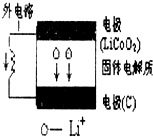
有关该电池的下列说法中,正确的是( )

有关该电池的下列说法中,正确的是( )
| A. | 电池内部“→”表示放电时Li+的迁移方向,外电路上的“→”表示放电时的电流方向 | |
| B. | 放电时负极的电极反应:LiCoO2-xe-═Li1-xCoO2+xLi+ | |
| C. | 充电时阴极的电极反应:6C+xLi++xe-═LixC6 | |
| D. | 当外电路有2 mole-通过,发生迁移的Li+的质量为7 g(Li的相对原子质量为 7) |
19.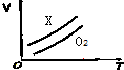 如图表示ag O2与a gX气体在恒压条件下的密闭容器中体积(V)与温度(T)的关系,则X气体可能是( )
如图表示ag O2与a gX气体在恒压条件下的密闭容器中体积(V)与温度(T)的关系,则X气体可能是( )
 如图表示ag O2与a gX气体在恒压条件下的密闭容器中体积(V)与温度(T)的关系,则X气体可能是( )
如图表示ag O2与a gX气体在恒压条件下的密闭容器中体积(V)与温度(T)的关系,则X气体可能是( )| A. | C3H6(气) | B. | CH4 | C. | CO2 | D. | NO |
3.25℃时,下列有关溶液中微粒的物质的量浓度关系错误的是( )
| A. | 0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-) | |
| B. | 0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3) | |
| C. | Na2C2O4溶液与HCl溶液等体积混合(H2C2O4是二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+) | |
| D. | 0.1mol/LNH4Cl与0.1mol/L氨水溶液等体积混合:c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) |
13.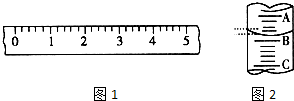 (1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在下表中填空,表示称量过程,并在图1所示的游码尺上画出游码的位置(画“|”表示).
(1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在下表中填空,表示称量过程,并在图1所示的游码尺上画出游码的位置(画“|”表示).
(2)图2表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量筒中的液体的体积是3.2mL.
(3)配制0.5mol•L-1的硫酸溶液200mL所需的玻璃仪器为量筒、烧杯、玻璃棒、200mL容量瓶、胶头滴管.
 (1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在下表中填空,表示称量过程,并在图1所示的游码尺上画出游码的位置(画“|”表示).
(1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在下表中填空,表示称量过程,并在图1所示的游码尺上画出游码的位置(画“|”表示).| 砝码质量/g | 50 | 20 | 20 | 10 | 5 |
| 取用砝码情况 |
(3)配制0.5mol•L-1的硫酸溶液200mL所需的玻璃仪器为量筒、烧杯、玻璃棒、200mL容量瓶、胶头滴管.
17.下列过程或现象与盐类水解无关的是( )
| A. | 纯碱溶液去油污 | B. | 明矾可作净水剂 | ||
| C. | 加热氯化铁溶液颜色变深 | D. | 硫酸氢钠溶液显酸性 |
18.A、B、C、D、E为原子序数依次增大的短周期主族元素,A与C、B与D分别同主族,且A、C元素的质子数之和是B、D元素质子数之和的一半.下列判断正确的是( )
| A. | 原子半径大小顺序:D>C>B>A | |
| B. | 由B和C元素组成的化合物,可以既含有离子键,又含有共价键 | |
| C. | 元素B、D、E分别与A形成的化合物中,熔沸点最低的是B与A形成的化合物 | |
| D. | 元素D与C形成的化合物在空气中长期放置不易变质 |