题目内容
1.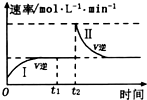 在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0; t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程(I、Ⅱ)如图所示.下列说法中,一定不正确的是( )
在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0; t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程(I、Ⅱ)如图所示.下列说法中,一定不正确的是( )| A. | 0~t1时,V正>V逆 | |
| B. | I、Ⅱ两过程分别达到平衡时,A的体积分数Ⅰ>Ⅱ | |
| C. | t2时刻改变的条件可能是向密闭容器中加C物质 | |
| D. | Ⅰ、Ⅱ两过程达到平衡时,平衡常数Ⅰ=Ⅱ |
分析 A、由图象分析可知,0~t1,反应正向进行,v正>v逆,t1~t2,反应到达平衡,v正=v逆;
B、由图象分析可知,t2时刻改变条件后达到平衡时,逆反应速率不变,说明和原平衡等效,体积分数不变;
C、向密闭容器中加C,逆反应速率瞬间增大,再次建立的平衡与原平衡等效,说明和原平衡相同;
D、由图象分析可知,t2时刻改变条件后达到平衡逆反应速率不变,说明和原平衡等效,则平衡常数不变;
解答 解:A、0~t1,反应正向进行,v正>v逆,t1~t2,反应到达平衡,v正=v逆,故A正确;
B、t2时刻改变条件后达到平衡时,逆反应速率不变,说明和原平衡等效,A的体积分数Ⅰ=Ⅱ,故B错误;
C、向密闭容器中加C,逆反应速率瞬间增大,再次建立的平衡与原平衡等效,说明和原平衡相同,符合图象,故C正确;
D、t2时刻改变条件后达到平衡逆反应速率不变,说明和原平衡等效,所以Ⅰ、Ⅱ两过程达到平衡时,平衡常数I=Ⅱ,故D正确;
故选:B.
点评 本题考查了化学平衡的建立,根据影响速率、平衡的因素来解答,注意图象的分析,难度中等.

练习册系列答案
相关题目
11.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| B. | 200mL1mol/LAl2(SO4)3溶液中,Al3+和SO42-离子总数为NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
9.“依靠科学,战胜非典”.以下是人们在面对“非典”时的一些认识,你认为符合科学道理的是( )
| A. | 家庭消毒时,消毒液越浓越好 | |
| B. | 烹饪时用“加碘食盐”可预防“非典” | |
| C. | 应经常保持室内清洁卫生和通风 | |
| D. | 必须每天吃药,补充人体所需化学物质 |
16.常温下,下列各组溶液充分混合后,混合液的pH一定小于7的是( )
| A. | pH=3的盐酸与pH=11的氨水等体积混合 | |
| B. | pH=5的溶液稀释至1000倍 | |
| C. | 0.2mol/L的酸性溶液与0.1mol/L的碱性溶液等体积混合 | |
| D. | pH=2的盐酸与pH=12的Ba(OH)2溶液等体积混合 |
6.如图所示的装置最适宜于干燥、收集的气体是( )


| A. | Cl2 | B. | NH3 | C. | NO | D. | NO2 |
13.只用一种试剂就能将AgNO3、KSCN、H2SO4(稀)、NaOH四种无色溶液区分开,这种试剂是( )
| A. | BaCl2 | B. | Ba(NO3)2 | C. | FeCl3 | D. | 盐酸 |
10.下列叙述不正确的是( )
| A. | 碳酸钠可以用于治疗胃酸过多 | |
| B. | 过氧化钠可做航天员的供氧剂 | |
| C. | 金属钠有强还原性,能和硫酸铜溶液反应,但不能析出金属铜 | |
| D. | 为使面包松软可口可用碳酸氢钠做发泡剂 |
11.下列变化,不能通过一步反应实现的是( )
| A. | Na2CO3→NaOH | B. | BaCl2→Ba(OH)2 | C. | FeCl3→Fe(OH)3 | D. | CaCO3→CaCl2 |